
QIAGEN甲基化panel第一篇文章近期发表在International journal of molecular science上,作者Muhammad Ahmer Jamil来自德国波恩大学,为了研究与血友病相关的肝窦内皮细胞的特点,作者分别对成年人和胎儿的肝窦内皮细胞以及其他内皮细胞进行转录组和甲基化测序,最终从基因表达和甲基化两个方面确定了相关生物标记物。
在甲基化研究中,作者先使用QIAseq Methyl Library Kit 进行全基因组甲基化测序,并确定了273个相关的甲基化区域,然后选择其中的6个区域使用QIAseq Targeted Methyl Panel对其中的CpG位点进行更精准的测序。这一研究思路与目前肿瘤早筛、慢病管理等甲基化研究思路均一致,也说明QIAGEN的新品QIAseq panel的特有优势,把握住了甲基化在疾病研究领域的火爆趋势,取得了更进一步的突破!并且使用QIAGEN的生信软件IPA在对f-LSEC和其他f-EC进行比较分析中确定的差异影响的典型途径。
在人类中,凝血因子VIII(F8)缺乏会导致A型血友病,而F8很大程度上是由肝窦内皮细胞(LSEC)合成和分泌的。但是,与其他内皮细胞相比,这些细胞的特异性和特征尚不清楚。在这项研究中,研究者进行了胎儿和成年人类原发性LSEC以及来自肺部(微血管和动脉)和心脏(微血管)的其他胎儿原代内皮细胞的全基因组表达和CpG甲基化分析。研究者的结果揭示了在胎儿和成年阶段区分LSEC的表达和甲基化标记。与其他胎儿内皮细胞相比,胎儿LSECs的差异基因表达指出了胎儿LSECs中的几种差异调节途径和生物功能。研究者使用有针对性的亚硫酸氢盐重测序,以确认选定的顶部差异甲基化区域。并进一步设计了一种检测方法,其中使用选定的甲基化标记物来测试内部iPS生成的血管内皮细胞与原发性LSEC的相似程度。发现与成人LSEC相比,胎儿具有更高的相似性。在这项研究中,研究者提供了LSEC的详细分子概况,并为测试体外分化LSEC产生的有效性提供了指导。
在这项研究中,研究者专注于将LSEC与其他EC进行比较,并对来自原代胎儿和成人LSEC以及其他胎儿EC的mRNA和CpGs甲基化进行了详细的分子分析。详细的分子分析产生了表达标志物,甲基化标志物和特定的分子/信号通路,从而将胎儿LSEC和成年LSEC彼此区分开,并与其他已研究的胎儿EC区分开。研究者详细的分子分析奠定了基础,并建立了将体外产生的EC与主要EC进行比较的工具。确实,我们产生了源自iPS的血管祖细胞EC(vEC),发现它们离胎儿比成年LSEC更近。
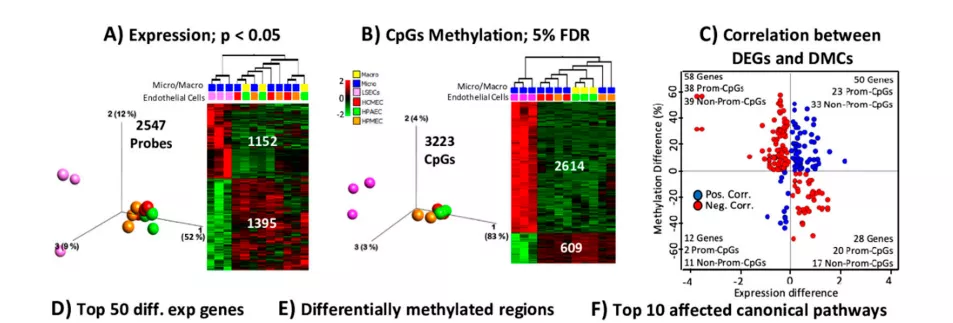

图1胎儿肝窦窦内皮细胞(f-LSECs)和其他胎儿内皮细胞的表达和CpGs甲基化分布图
细胞(f-ECs):人心脏微血管内皮细胞(HCMEC),人肺动脉内皮细胞(HPAEC)和人肺微血管内皮细胞(HPMEC)。(A)差异表达基因(DEGs)(p <0.05)和(B)差异甲基化CpGs(DMCs)(FDR的5%)的三维PCA图和热图。(C)DEG(p <0.05)和CpG甲基化之间的相关性(Pearson> 0.7)(红色和蓝色分别对应负相关和正相关)。(D)-log10(p)的热图和f-LSEC和f-EC之间的前50个DEG的平均表达差异(log2标度的倍数变化)(基于绝对平均表达差异的前8个DEG的个体数据)显示在框中情节)。(E)比较f-LSEC和其他f-EC的所有差异甲基化区域的热图。(最好的六个基因座的个人数据显示在方框图中。)(F)与f-LSEC和其他具有大量上调和下调基因的f-EC相比,十个受影响的经典途径富含DEG。(G)IPA在对f-LSEC和其他f-EC进行比较分析中确定的差异影响的典型途径。仅显示那些显示相同的Z分数比较方向的人(即,与f-LSEC相比,所有Z分数为负或正)。
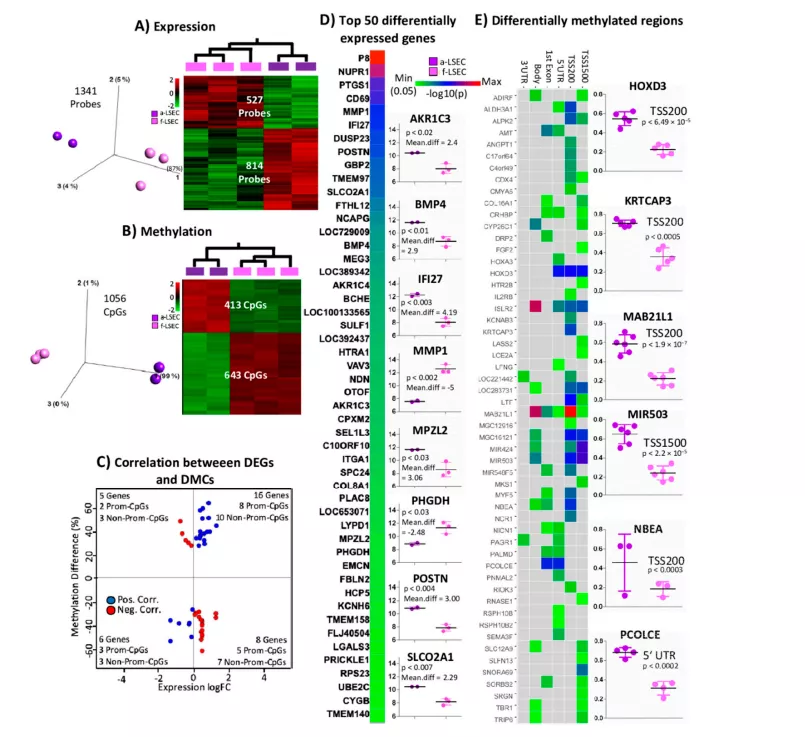
图2. 在成年和胎儿肝窦窦内皮细胞(a-LSEC,f-LSECs)中的表达和CpGs甲基化分布图
(A)差异表达基因(DEGs)(p <0.05)和(B)差异甲基化CpGs(DMCs)(在FDR的5%和0.3投影得分时)的3D-PCA图和热图LSEC。(C)DEG(p <0.05)和CpG甲基化之间的相关性(Pearson> 0.7)(红色和蓝色分别对应负相关和正相关)。(D)-log10(p)的热图和a-LSEC和f-LSEC之间的前50个DEG的均值差(log2标度的倍数变化)(方框图表示基于绝对均值表达差异的前8个显着位点)。(E)关于基因的不同区域(即TSS1500,TSS200、5'UTR,1stExon,body,3'UTR),a-LSEC和f-LSEC之间的差异甲基化区域(DMR)比较的热图(箱图代表六个最重要的标记)。
虽然Illumina阵列提供了经济高效且技术含量较低的优点,但这些阵列的缺点是只能覆盖一小部分的基因组CpG。整个基因组亚硫酸氢盐测序(WGBS)方法克服了这一低的基因组覆盖率,并具有覆盖基因组中可能遗漏或未被阵列覆盖的每个CpG位点的潜力。研究者发现a-LSEC和f-LSEC之间没有全基因组意义(图3 A)。在5%FDR的情况下,他们确定了273个DMC(图3 B)。Illumina EPIC阵列与QIASeq甲基WGBS之间的相关性表明,两种LSEC(成人和胎儿)的预期高度显着相关性都超过90%(图3C)。此外,根据他们识别DMR的方法,在a-LSEC和f-LSEC之间发现了25个重要的DMR;选择了六个DMR作为有效标记(图3 D),包括MGMT,CTSZ和NACC2基因中的区域。
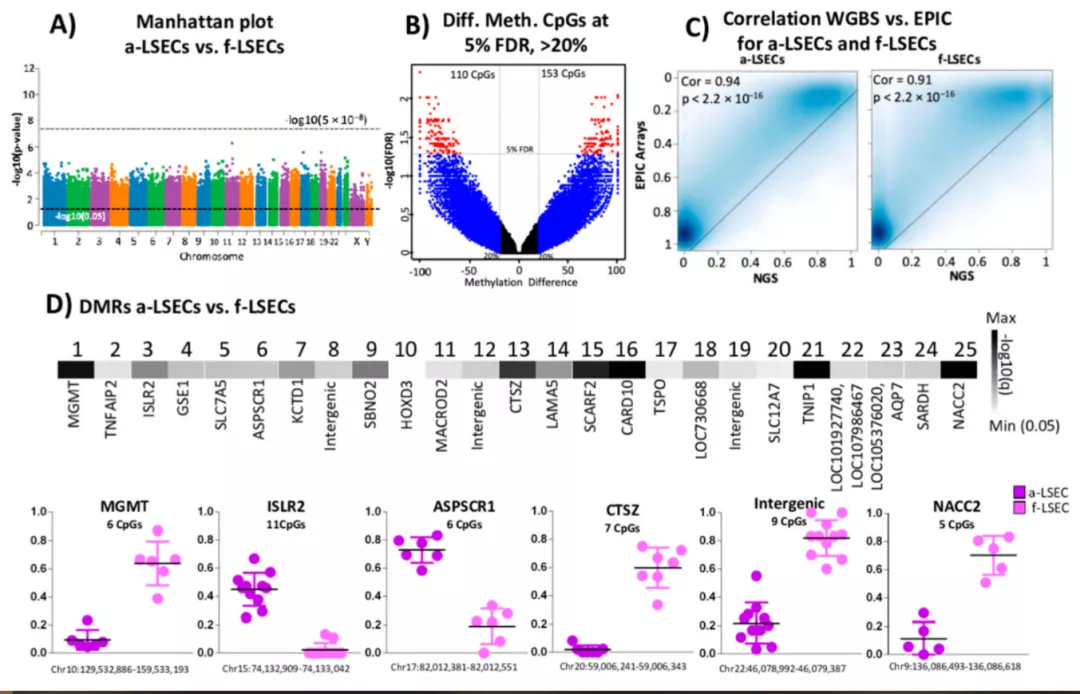
图3. 成年和胎儿肝窦窦内皮细胞(a-LSEC,f-LSEC)之间的全基因组亚硫酸氢盐测序数据分析
(A)a-LSEC和f-LSEC之间–log10(p)的全基因组曼哈顿图。(B)a-LSEC和f-LSEC之间的甲基化差异和–log10(FDR)的火山图。(C)成人和胎儿LSEC中Illumina EPIC甲基化和QIASeq甲基全基因组亚硫酸氢盐测序数据之间的相关性和密度图。(D)a-LSEC和f-LSEC之间的重要差异甲基化区域(DMR)的热图。下面的方框图显示了选定DMR中a-LSEC和f-LSEC的个别CpGs甲基化。
研究者从三个基于甲基化的比较中分别选择了六个区域(A. f-LSEC与其他胎儿(图1 E),B。f-LSEC与a-LSEC在阵列中(图2 E)和C. f- WGBS中的LSEC到a-LSEC(图3 D)),可通过有针对性的亚硫酸氢盐重测序进行验证,从而对单个DNA分子进行测序,揭示了甲基化的细节以及相邻CpG之间表观遗传变化的阶段。使用这种方法,他们能够生成覆盖258个CpG的16个区域的实验数据。作为3D-PCA分析的结果,第一组在四个区域(1:CDH5、3:GSTO2、5:RABGGTA和6:ZC3H12D)显示26个CpG,样品之间的分离度为ANOVA p <0.05(图4,左侧)。基于第二组,四个区域(7:HOXD3、9:MAB21L1、10:MIR503和12:PCOLCE)中的98个CpG清楚地将成年LSEC与其他细胞类型分开(图4,中间部分)。第三组在五个区域(13:MGMT,15:ASPSCR1、16:CTSZ,17:基因间区域和18:NACC2)中发现了53个CpG,并将a-LSEC与其他样品清楚地分开(图4,右上部分)。作为上述分析的结果,研究者建议在七个区域(3:GSTO2、5:RABGGTA,6:ZC3H12D,7:HOXD3、12:PCOLCE,13:MGMT和18:NACC2)中建立一个特别有效的区域并将成人和胎儿的LSEC与其他EC进行区分(图4,下部)
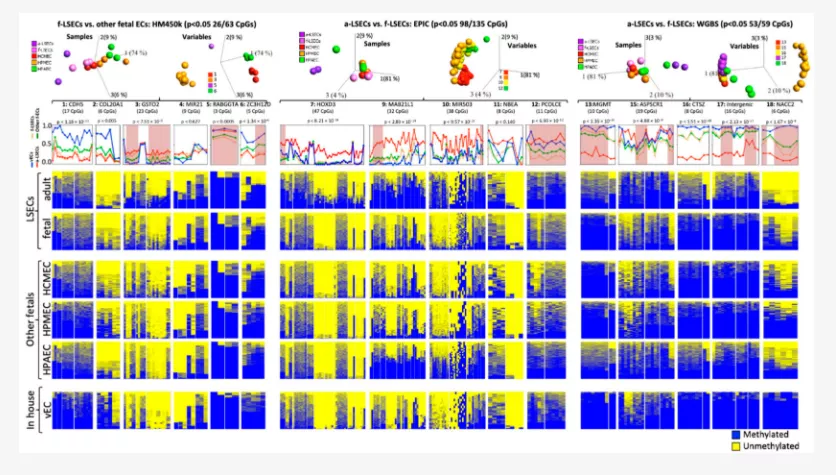
图4. 不同内皮细胞中的靶向亚硫酸氢盐重测序
分析16个选定区域的统计显着性,将成人和胎儿肝窦窦内皮细胞(a-LSEC和f-LSECs)与其他胎儿内皮细胞(f-ECs)进行比较。顶部面板:p处选定区域的样本和变量的PCA图<0.05。以下是差异甲基化区域(DMR)的基因宿主的名称,其后是代表a-LSEC,f-LSEC,f-EC和血管内皮细胞(vEC)区域中所有CpG的平均甲基化的线图。(有权清楚区分a-LSEC,f-LSEC和其他f-EC的区域以橙色突出显示)。底部是a-LSEC,f-LSEC,f-ECs(人心脏微血管内皮细胞(HCMEC),人肺微血管内皮细胞(HPMEC)和人肺动脉内皮细胞(HPAEC))和vEC。
总之,在这项研究中,研究者将LSEC的分子特征(表达和DNA甲基化)与选定的vEC进行了比较。揭示了胎儿LSEC的几种生物学指纹,例如FCN3,IGFBP5,DNASE1L3,THY1和H19的相对较高表达,而MGP,EFEMP1和POSTN的较低表达。此外,LSECs的特征是抑制EIF2和mTOR信号通路。最后,在LSEC中鉴定出一组DMR,这些DMR可用于表征体外衍生的LSEC。与其他vEC相比,研究者的研究首次表征了LSEC。
全基因组甲基化建库QIAseq Methyl Library Kit
Cat No./ID: 180502
用于DNA甲基化分析的强大文库制备
高文库产率和作图率
低偏倚和错误率
DNA输入的宽范围
与cfDNA样品兼容
适用于富集的片段化样品(例如RRBS,MeDIP)
甲基化靶向建库QIAseq Targeted Methyl Panels
Cat No./ID: 335501
具有唯一分子条形码(UMI)的错误校正可增强NGS芯片灵敏度
与其他NGS技术相比,单端特异性引物扩增(SPE)方法可提高灵敏度并克服靶向挑战
可使用QIAGEN GeneGlobe或本地安装的QIAGEN CLC Genomics Workbench软件
QIAseq靶向甲基化建库的Sample to Insight分析解决方案提供了一种能够针对基因组中数千个CpG位点的单次解决方案。与靶向DNA芯片一样,QIAseq解决方案基于单引物延伸(SPE)技术,可为检测整个基因组区域提供灵敏而特异的解决方案。
差异表达基因功能挖掘软件QIAGEN Ingenuity Pathway Analysis (IPA)

IPA 是一款基于云端的工具,可以进行组学数据的分析、整合和解读。支持的数据类型包括 RNAseq、Microarray、miRNA、SNP、代谢组学、qPCR 和化合物等。IPA 基于强大的 Knowledge Base 可以挖掘组学数据对应的生物学功能、鉴定新的靶标或潜在的生物标志物。
IPA 功能:
• 经典通路富集:鉴定显著富集的生物学通路,基于表达值预测对该通路是激活还是抑制
• 上游调控因子:鉴定上游调控因子,包括 miRNA、转录因子、药物、酶等
• 因果关系网络:构建多层调控网络,挖掘新的调控机理和主调控因子
• BioProfiler:通过搜索 Knowledge Base,构建疾病相关的分子图谱,包括基因、药物等信息
• 调控机理网络:自动构建信号调控级联,挖掘导致基因表达变化的分子机理
• 分子活性预测:预测网络中核心分子的激活或抑制对上下游分子的影响
• 相互作用网络:构建转录调控网络、miRNA-mRNA 网络、磷酸化级联网络等分子网络
• 匹配分析:自动将分析结果与已有的分析结果或 8000+ 个公共数据库中的人和小鼠表达数据分析结果进行匹配分析,
找到相似或相反的结果
• 磷酸化分析:鉴定网络中导致蛋白磷酸化水平变化的上游调控因子或主调控因子
• MicroRNA:基于 TarBase、miRecords、TargetScan 以及文献信息快速过滤 microRNA-mRNA 配对










 危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)
危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)  营业执照(三证合一)
营业执照(三证合一)