•所谓“不可成药(undruggable)”,常用来描述传统药物研发中那些因结构和功能特征而难以成为用药靶点的蛋白质。
•最近,美国食品和药物管理局(FDA)加速批准了一种用于治疗NSCLC的KRAS抑制剂,KRAS就是“不可成药”基因的一个典型例子。
•PROTAC技术可以成为开发针对“不可成药”基因的有效疗法的有力工具。
二十年前,在人类基因组计划第一版发表后不久,霍普金斯和格鲁姆(1)提出了“可成药性”的概念。他们估计,在30,000个预测的人类蛋白质编码基因中,只有约15%有可能成为可利用的药物靶点,这意味着其余85%的蛋白质组被认为是无法用药的。科学的进步使这两类基因之间的区别越来越模糊,许多最初被认为无法用药的基因实际上已经成功地成为靶点(如BCL-2家族成员)。
好的治疗靶点有哪些特征?
1. 功能/活性。必须从一系列疾病或症状的驱动因素中选择潜在的靶蛋白。历史上,典型的药物靶点包括G蛋白偶联受体(GPCR)、核受体、离子通道和酶,因为它们具有“活性”功能,更容易击中。随着时间的推移,具有不同功能的蛋白质,如参与特定蛋白质-蛋白质相互作用(PPI)的蛋白质以及支架蛋白和结构蛋白越来越多地被视为潜在靶标(2)。一个隐患是,与疾病相关的蛋白质通常在健康细胞和组织中具有非病理性活性。因此,一味抑制它们的功能可能会导致不必要的副作用。
2. 表达。与前述观点一致,理想的候选蛋白质不应普遍表达,因为当“功能障碍”主要定位于特定组织时,发生脱靶效应的风险较低。考虑到药物开发的主要瓶颈之一是脱靶效应,脱靶效应会导致与剂量相关的毒性和/或剂量有限的疗效,因此这一点尤为重要。为了克服这一困难,大量研究人员致力于开发专门针对相关细胞的给药策略(如基于抗体、肽、适配体的给药策略)(3)。
3. 可及性。组织和细胞蛋白质的表达部位也与治疗药物能否轻易到达有关。例如,血脑屏障使大脑相对难以进入。因此,任何试图攻击神经元蛋白质的尝试都需要考虑这一障碍。此外,蛋白质对特定药物的可及性还取决于其在细胞水平的位置(如细胞表面、细胞质、细胞核/其他细胞器、细胞外环境)。例如,治疗性抗体可以到达蛋白质的细胞外部分,而细胞内靶点则需要能够穿透细胞的小分子化合物。
4. 结构。从历史上看,当蛋白质具有疏水结合袋和/或--在酶的情况下--明确的活性位点,可以容纳候选药物时,蛋白质就被认为是可药用的。相反,信号分子、结构蛋白等的活性通常依赖于蛋白质与蛋白质之间的相互作用,因此依赖于其三级或四级结构的变化。这种内在的可变性和缺乏确定的沟槽使得识别潜在药物的结构和物理特征(如大小、极性等)变得更加困难。
5. 结合亲和力。与酶抑制特别相关,它表示酶识别特定底物的能力:亲和力越高,结合能力越强,即使底物浓度很低。对底物具有高亲和力的酶是更棘手的药物靶点,因为潜在抑制剂需要极高浓度(有时甚至是不可行的浓度)才能与底物竞争。
不可成药的癌症基因
癌症是导致全球死亡的主要原因之一(4),因此开发有效的治疗方法是药物发现活动的主要目标之一。癌症类型和病因的多样性使得这项工作尤为复杂。在已发现的700个癌症基因中,目前仅有约40个基因的治疗方法获得批准(5)。此外,大多数研究工作往往集中在一组有限的“易药”蛋白上(如HER2、EFGR、ALK、PD-1/PD-L1、雌激素受体或雄激素受体),因此,对于同一靶点,无论其在癌症发生或发展中的实际发生率如何,都有多种FDA批准的药物可用。例如,虽然“仅”在3%-5%的非小细胞肺癌中发现的ALK基因重排有五种已获批准的治疗方法(5,6),但绝大多数最常见的癌基因改变直到最近仍被认为是“不可成药”的。
RAS、MYC和TP53就是典型的例子。事实上,RAS是癌症中最常见的突变癌基因,MYC是最常见的扩增癌基因,而TP53则是最常见的突变和/或删除肿瘤抑制基因(5)。这些基因突变是如此常见,以至于在任何人类癌症中都有可能发现其中至少一种基因突变。不过,上一段中提到的几个特征也适用于这些蛋白质。例如
•它们表达广泛,对细胞的正常功能起着关键作用,因此脱靶风险很高。
•它们位于细胞内部(尤其是P53和c-Myc),因此更难到达。
•它们没有一个明确的口袋,潜在的低分子量药物无法与之结合。
•c-Myc是一种内在无序蛋白(IDP),具有扩展的非结构化表面,因此缺乏常规药物的靶“热点”。
•P53和MYC没有酶活性,因此不能使用催化抑制剂。
•RAS具有内在的GTP酶活性,但其对GTP的高亲和力和细胞内GTP浓度的升高使得开发竞争性抑制药物的可能性很小。
然而,尽管这些基因被称为“不可成药的基因”,但最近的研究进展使得潜在的治疗策略得以开发,并在最近取得了突破性进展:2021年5月,美国食品和药物管理局(FDA)加速批准RAS GTPase家族抑制剂索托拉西布(Sotorasib)用于治疗KRAS G12C突变的转移性非小细胞肺癌(NSCLC)成人患者(7)。
靶向KRAS的成功案例
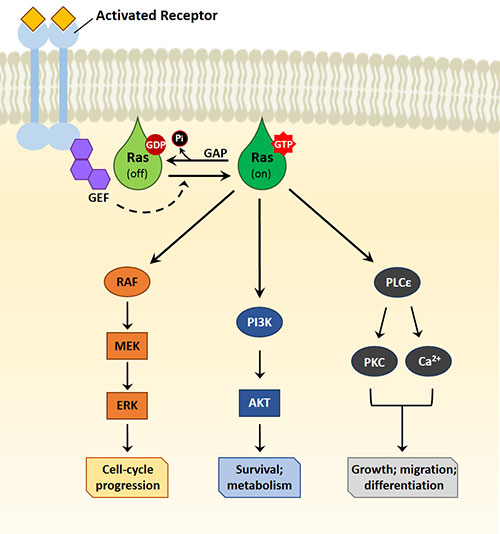
1. Ras家族Ras。蛋白家族由三个同源基因编码,即HRAS、KRAS和NRAS,代表了一些最早被描述的致癌基因。它们最初在60年代被发现是诱发大鼠肉瘤的病毒成分(因此被称为RAS:大鼠肉瘤病毒),它们的发现改变了我们对癌症生物学的认识(7、8、9)。Ras蛋白属于G蛋白(鸟苷酸核苷酸结合蛋白)类。它们以GTP结合的活性形式和GDP结合的非活性形式交替发挥作用,就像多个信号通路的开关一样(7)。所有三种形式的Ras都是膜相关蛋白,附着在细胞膜上对它们的功能至关重要。在静止细胞中,Ras蛋白与GDP结合。受体酪氨酸激酶(RTKs)或GPCRs等各种膜受体可激活Ras信号传导,这些受体与配体相互作用后,会将鸟嘌呤核苷酸交换因子(GEFs)招募到膜上,进而诱导GDP与Ras分离。在短暂的无核苷酸状态之后,Ras与GTP结合,进入其活性状态,在这种状态下,它可以与各种效应蛋白相互作用,诱导不同的细胞反应。图1描述了Ras下游的主要通路,如参与细胞周期进展的RAF/MAPK/ERK 通路;参与细胞存活和代谢调节的PI3K/AKT信号通路;参与细胞生长、分化和迁移的 PLCε/PIP2 级联通路。在正常细胞中,Ras会被称为GTP激活蛋白(GAP)的调节蛋白关闭,GAP会加速GTP的水解,使Ras转变为无活性的GDP结合态。
图1 Ras信号通路
RAS基因发生致癌突变后,最常见的后果之一就是对GAP产生抗性,从而持续处于活性状态。约30%的人类癌症中都存在RAS基因突变,其中KRAS基因突变最常见(约占80%),其次是NRAS(12%)和HRAS(3%)(5)。KRAS密码子12和13都编码甘氨酸残基,是最常见的致癌激活位点,90%以上的记录突变都发生在这些位点上。这些残基与GDP/GTP结合袋相邻。甘氨酸与其他氨基酸的替换会干扰GTP酶的活性,甚至在GAPs结合后也会将KRas锁定在 GTP结合的活性状态(11)。
2. 针对Ras的治疗。鉴于RAS基因突变在人类癌症中的发生率很高,多年来,人们一直在努力开发能够对抗RAS基因突变的药物。下面仅列举几个例子。有人尝试抑制负责前炔化的酶,前炔化是Ras与细胞膜内层结合所需的翻译后修饰。目前有几种药物正在进行临床试验,其中一种名为Tipifarnib的药物获得了美国食品及药物管理局(FDA)的“快速通道”认证,用于治疗HRAS突变的头颈部鳞状细胞癌和T细胞淋巴瘤患者(5)。
另一种流行的策略是尝试抑制下游信号传导,即通过抑制通路的效应因子(如RAF/MEK/ERK或PI3K/Akt),或直接阻止Ras与这些效应因子的相互作用。到目前为止,第一种策略并没有取得令人鼓舞的结果,这可能是由于细胞采用了代偿机制。相反,Rigosertib作为一种Ras拟态化合物,似乎能够阻断Ras效应器的下游信号传导,从而抑制临床前模型中的肿瘤生长(5、12)。该分子目前正在进行多项临床试验。
最后,有关Ras突变体的结构信息使我们能够直接靶向Ras突变体。特别是 KRAS G12C(其中一个半胱氨酸残基取代了由密码子12编码的甘氨酸)显示了一个调节袋,人们利用这个调节袋开发出了对野生型RAS没有检测到影响的特异性抑制剂。其中,前面提到的Sotorasib(原名AMG510)是第一个获得 FDA 批准的KRAS阻断药物。它能选择性地、不可逆地抑制突变蛋白,并将其锁定为无活性的GDP结合形式,从而使KRAS G12C肿瘤消退,并提高化疗的抗肿瘤疗效(13)。在临床试验“CodeBreak100”中,Sotorasib使36%的参与者的肿瘤缩小(相比之下,标准疗法的肿瘤缩小率为20%)。这些肿瘤反应的中位持续时间为10个月(而标准疗法的预期寿命较短)(14)。与其他任何药物治疗一样,Sotorasib也会产生一些副作用,大多数情况下副作用较轻(如腹泻、恶心、肌肉和骨骼疼痛),但有20%的参与者副作用较重。由于Sotorasib这么快就获得了美国食品药品管理局的加速批准,目前仍在进行更多的试验,以确认该疗法是否能帮助NSCLC患者延长寿命,而不会导致癌症恶化(14)。希望这一成功故事不仅能在其他已在临床试验中的类似抑制剂中复制,而且还能促进针对不同KRAS突变的化合物的开发。
PROteolysis-TArgeting Chimaera(PROTAC)技术:挑战“不可成药”靶点
如上所述,尽管取得了令人鼓舞的重要科学进步,但药物发现仍然在很大程度上依赖于使用能够占据目标蛋白质上特定活性位点、直接影响其功能的分子。因此,在缺乏这些确定区域的情况下,很难制定出适当的策略。
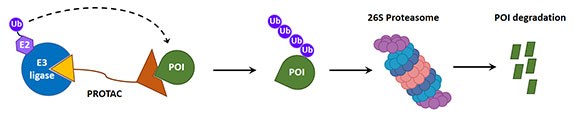
在这种情况下,最近开发出了多种杂多功能分子,它们将一种能结合感兴趣的蛋白质(POI)的配体与另一种能与E3泛素连接酶结合的配体绑在一起,促进前者的泛素化,然后由26S蛋白质体降解,这可能会对“给“无法药用”的基因下药”产生重大影响。这些异功能分子被称为PROteolysis-TArgeting Chimeras或PROTACs15(图 2)。
图2 PROTACs机制
PROTACs不需要基因修饰(不同于其他技术,如RNAi或基因KO);不需要 POI上存在活性位点;使用浓度比传统小分子低,因为与靶点的瞬时相互作用就足以将其导向蛋白酶体;它们还适用于通过过表达克服抑制剂作用的靶点,如癌症中经常出现的靶点(15、16)。例如,BRD4是一种转录和表观遗传调控因子,通过激活多个癌基因(如c-Myc)的转录,在癌症发展中发挥着关键作用。BRD4抑制剂会因BRD4表达增加而迅速失去药效,而BRD4-PROTACs则不受这种机制的影响(16、17)。
Enzo life的PROTACs以表皮生长因子受体(EGFR)和BET溴域蛋白(如A1874)为靶标。这是一种基于坚果素的PROTAC,靶向BRD4,因此由BRD4配体(JQ1)与MDM2 E3配体(RG7388)连接组成。正如Hines J等人最近证明的那样(15),A1874具有双重功能,它能诱导其靶标降解,并伴随着c-Myc的下调、P53的稳定和P21的上调。
药物发现的研究工具:
• SCREEN-WELL® Cancer Library和SCREEN-WELL® Kinase Inhibitor library等化合物库可以成为癌症抑制剂筛选和药物开发的强大工具。
• AKT、PKA和PKC检测试剂盒可以通过分析样品中的致癌信号变异来补充筛选工作。
• CELLESTIAL®目录中的荧光探针可对细胞内反应(如细胞凋亡/坏死、细胞毒性、氧化应激、细胞器功能动态等)进行动态分析。
参考文献:
1. Hopkins AL & Groom CR. The druggable genome. Nat Rev Drug Discov (2002). PMID: 12209152.
2. Ghadermarzi S, et al. Sequence-Derived Markers of Drug Targets and Potentially Druggable Human Proteins. Front Genet (2019). PMID: 31803227.
3. Zhao Z, et al. Targeting Strategies for Tissue-Specific Drug Delivery. Cell (2020). PMID: 32243788.
4. World Health Organization, Cancer - Key Facts.
5. Duffy MJ & Crown J. Drugging "undruggable" genes for cancer treatment: Are we making progress? Int J Cancer (2021). PMID: 32638380.
6. Rosas G, et al. ALK rearrangements: biology, detection and opportunities of therapy in non-small cell lung cancer. Crit Rev Oncol Hematol (2019). PMID: 30878128.
7. Nakajima EC, et al. FDA Approval Summary: Sotorasib for KRAS G12C-Mutated Metastatic NSCLC. Clin Cancer Res (2022). PMID: 34903582.
8. Gimple RC & Wang X. RAS: Striking at the Core of the Oncogenic Circuitry. Front Oncol (2019). PMID: 31681559.
9. Harvey JJ. An unidentified virus which causes the rapid production of tumors in mice. Nature (1964). PMID: 14243400.
10. Kirsten WH & Mayer LA. Morphologic responses to a murine erythroblastosis virus. J Natl Cancer Inst (1967). PMID: 18623947.
11. Naguib A, et al. Activation of K-RAS by co-mutation of codons 19 and 20 is transforming. J Mol Signal (2011). PMID: 21371307.
12. Atuluri-Divakar SK, et al. A small molecule RAS-mimetic disrupts RAS association with effector proteins to block signaling. Cell (2016). PMID: 27104980.
13. Canon J, et al. The clinical KRAS(G12C) inhibitor AMG 510 drives anti-tumor immunity. Nature (2019). PMID: 31666701.
14. NCI Staff. FDA Approval of KRAS Inhibitor Sotorasib for Lung Cancer Hailed as Milestone. Cancer.gov (2021).
15. Hines J, et al. MDM2-recruiting PROTAC Offers Superior, Synergistic Anti-proliferative Activity via Simultaneous Degradation of BRD4 and Stabilization of p53. Cancer Res (2019). PMID: 30385614.
16. Dang CV, et al. Drugging the 'undruggable' cancer targets. Nat Rev Cancer (2017). PMID: 28643779.
17. Lai AC & Crews CM. Induced protein degradation: an emerging drug discovery paradigm. Nat Rev Drug Discov (2017). PMID: 27885283.
文中部分相关产品:
关于Enzo Life
Enzo Life做为分子诊断领域的先驱者,可提供包括基因、蛋白、细胞、组织全层面的标记和检测试剂,如原位杂交探针、活细胞荧光探针、组化试剂盒、小分子化学文库等。除了科研领域外,Enzo Life还给提供多样的生物工艺质量检测试剂盒(如Protein A残留检测盒,HCP残留检测等 )










 危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)
危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)  营业执照(三证合一)
营业执照(三证合一)