Science揭示巨噬细胞kupffer的新帮手,原来竟是他?!
时间:2023-11-09 10:23:38 浏览次数:3145
2023年的国自然热点,巨噬细胞凭借822个中标量荣登榜首,近三年的热度也持续攀升。命运图谱模型(fate-mapping)、转录组学等技术的不断进步推动了揭开组织驻留巨噬细胞神秘面纱的脚步。今年6月,Frederic Geissmann团队在nature发表了名为《Physiology and diseases of tissue-resident macrophages》,针对这些年组织驻留巨噬细胞的起源以及在不同组织或者生理过程中发挥的功能进行总结(感兴趣的伙伴可以点击标题阅读原文)。九月,Paul Kubes团队找到了肝纤维化病理状态下组织驻留巨噬细胞的新帮手及其具体机制(本次精读的文章,原文链接也在这里呦),巨噬细胞的研究进展如此可喜,快来和小优一起看看吧!

Kupffer细胞样合胞体代偿纤维化肝脏中常驻巨噬细胞的功能

文章概览:
肝脏中的常驻巨噬细胞在与肝细胞、内皮细胞和星状细胞组成的龛位中接受指令,进而激活特定的转录因子,赋予其新身份:Kupffer细胞(KC)。在血窦中,KC向实质细胞延伸伪足以保持其特性,充当人体的中央细菌过滤器,并且通过补体受体CRlg在内的特异性受体,发挥从血液中捕捉病原体的功能。肝纤维化和肝硬化的发展过程十分相似,均会涉及肝细胞死亡和肝窦周围的胶原沉积导致血流重新分配到新的和扩张的肝内和肝外侧支血管。然而在这种组织重塑过程中,KC如何适应变化尚未可知。
在这项研究中,作者观察、追踪并功能性评估了肝纤维化状态中的单核细胞和KC:在纤维化龛中失去与实质细胞的接触会导致窦状驻留的KC失去特性和功能,而单核细胞会跟随侧支血管的形成绕过窦,在窦中形成类似KC的合胞体,表达KC细胞标记,具有更强的捕捉细菌的能力,从而挽救并适应肝纤维化状态中下调的KC细胞的功能特性(图1)。这些细胞结构可能在进化过程中发挥了关键作用,使哺乳动物能够承受肝脏中严重的慢性损伤。这项研究成果有望改进肝纤维化患者的治疗方案。
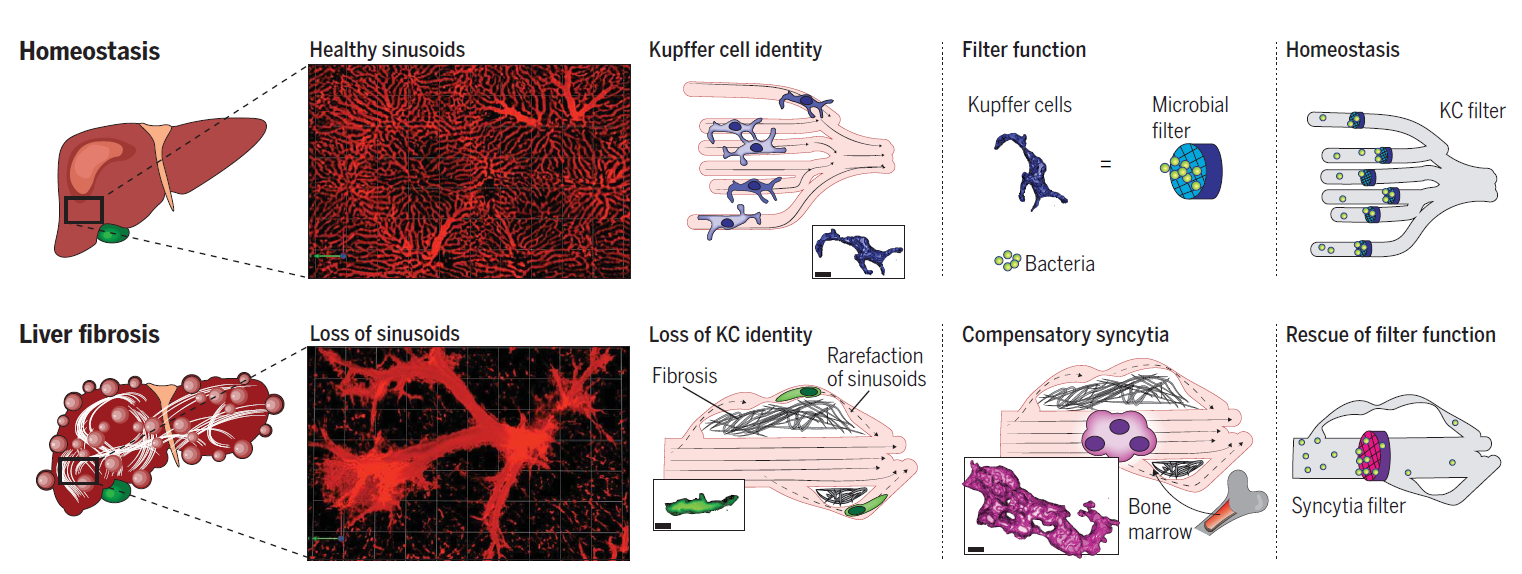 图1 肝纤维化中KC的适应变化
图1 肝纤维化中KC的适应变化
主要结果:
01 Kupffer细胞的免疫监视功能及肝纤维化的进行性血管重塑
与其他免疫细胞不同的是,KC向实质细胞(肝星状细胞、肝窦内皮细胞、肝细胞)延伸伪足,形成KC龛(图2A-B),两者之间的相互作用对于维持KC细胞的功能十分重要,这种生态位也是免疫监视的最佳选择,如小鼠感染葡萄球菌(MW2-GFP)后,KC能够迅速捕获细菌,并且为了KC能够迅速占据大量窦腔,窦道会变得足够狭窄(图2C)。
 图2 Kupffer细胞的免疫监视功能及肝纤维化的进行性血管重塑
图2 Kupffer细胞的免疫监视功能及肝纤维化的进行性血管重塑
部分相关产品:
| 货号 | 产品名称 | 规格 |
| NB600-404APC | Rat Monoclonal F4/80 Antibody (CI-A3-1) [Allophycocyanin] | 0.125ml |
| MAB5580-SP | Mouse F4/80 Antibody | 25ug |
| MAB2145-SP | Mouse CXCR6 Antibody | 25ug |
| AF3628-SP | Mouse/Rat CD31/PECAM-1 Antibody | 25ug |
02 肝纤维化改变了Kupffer细胞的生态位,导致其功能丧失
明确了KC的免疫监视功能之后,作者接下来研究了在肝纤维化病理状态下的KC生态位。与正常小鼠相比,CCl4建立的小鼠肝纤维化模型中,肝窦周围有大量的胶原沉积,肝血流量也降低(图3A-D),并且肝窦的直径减小,KC的伪足也明显减少(图3E-F),不仅如此,与健康受试者相比,肝硬化(F4期纤维化)患者的KC平均数也降低(图3G-H)。进一步地,作者证实了KC与造血干细胞之间的共定位(图3I)。感染金黄色葡萄球菌后,与对照组小鼠相比,肝纤维化小鼠肝窦中KC的细菌捕获明显减少,在捕获细菌的窦液中,F4/80+巨噬细胞的比例也有所下降,同时血液及脾脏中的细菌负荷也明显高于对照组(图3J-L)。由于KC也能够杀死捕获的葡萄球菌,接下来作者对两组小鼠KC的吞噬能力进行测定,与对照组相比,CCl4处理后,对捕获异物的酸化处理延迟了一个小时(图3M),这表明,肝纤维化环境中KC的抗菌能力下调甚至丧失。
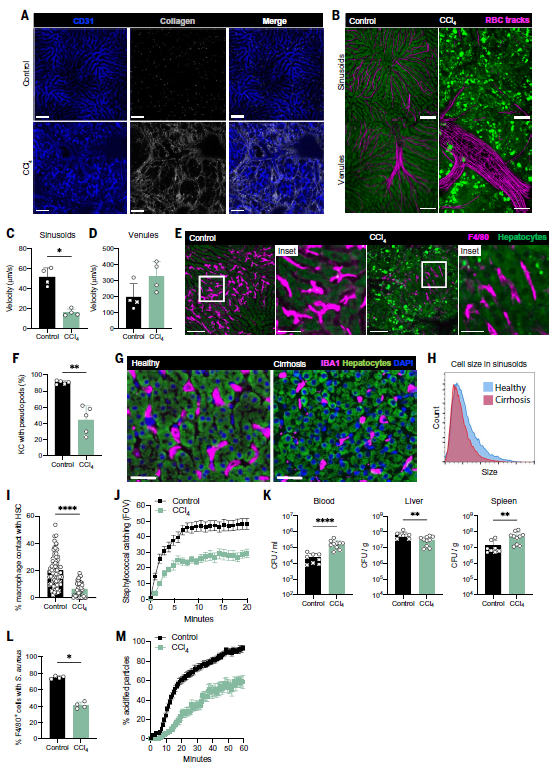 图3 肝纤维化改变了Kupffer细胞的生态位,导致其功能丧失
图3 肝纤维化改变了Kupffer细胞的生态位,导致其功能丧失
部分相关产品:
| 货号 | 产品名称 | 规格 |
| 48934S | Iba1/AIF-1(E4O4W)XP® Rabbit mAb(Alexa Fluor® 594 Conjugate) | 100ul |
| 17198T | Iba1/AIF-1(E4O4W)XP® Rabbit mAb | 20ul |
| 10513S | Iba1/AIF-1(E4O4W)XP® Rabbit mAb(PE Conjugate) | 100ul |
03 肝纤维化导致Kupffer细胞特性丧失
由于纤维化肝窦中巨噬细胞丧失KC特性,作者接下来重点研究了赋予KC表型适应性的两个关键分子:免疫球蛋白超家族互补受体(CRIg)和T细胞膜蛋白4(TIM-4)。与对照组小鼠相比,CCl4处理后,表达TIM-4和/或CRIg的F4/80+巨噬细胞明显减少,并且四种KC识别标记物(CLEC2、CLEC4F、CRIg和TIM-4)的水平也显著降低(图4A-D)。在肝硬化患者的活检组织中也观察到了,IBA1+(IBA1可识别所有巨噬细胞)人肝窦巨噬细胞中CRIg的丢失(图4L-M)。为了研究肝窦KC的发育,作者使用了Ms4a3cre×Rosatdtomato单核细胞命运图谱小鼠,其骨髓(BM)衍生的前体而非胎肝衍生的常驻巨噬细胞会发出荧光。稳态条件下,肝窦中2-10%巨噬细胞来自BM来源的单核细胞。经过8周的CCl4处理后,窦腔中约30%的巨噬细胞来自BM来源的单核细胞,70%来自胎肝来源的KC,(图4E-F)。将来源于BM的Ms4a3+F4/80+细胞和来源于胎肝的Ms4a3-F4/80+细胞分类为表达CRIg和TIM4的细胞,结果显示这些标记在胎肝细胞和来源于BM的细胞中的比例相似,这表明KC在纤维化过程中正在发生去分化(图4G)。
此外,F4/80+CRIg+TIM-4+细胞的Ms4a3比例最低,但F4/80+CRIg+TIM-4-细胞和F4/80+CRIg-TIM-4-细胞的单核细胞替代率低于50%(图4H)。8周的CCl4处理后,宿主CK也降低了10%左右(图4I)。Clec4fcre-nTdTomato×Rosa26ZsGreen小鼠中,窦道中超过95%的F4/80+细胞共表达了tdTomato和ZsGreen,表明KC表型活跃,然而CCl4处理后,肝窦中存在三种F4/80+细胞亚群:tdTomato+ZsGreen+KCs、tdTomato-ZsGreen+前KCs(exKCs)和无CLEC4F表达的F4/80+细胞(图4J)。这表明KC细胞下调的标记物,除了CRIg和TIM4,还有CLEC4F。并且,CCl4处理后ZsGreen+tdTomato+F4/80+KC的细菌捕获能力更强(图3K)。这表明,即使在纤维化过程中,也需要KC表型来捕获细菌。
 图4 肝纤维化导致Kupffer细胞特性丧失
图4 肝纤维化导致Kupffer细胞特性丧失
部分相关产品:
| 货号 | 产品名称 | 规格 |
| FAB4646S-100UG | Human VSIG4 Alexa Fluor750-conjugated Antibody | 100ug |
| 75484T | TIM-4(D3W4F)XP® Rabbit mAb | 20ul |
04 纤维化中出现多核合胞体,Kupffer细胞特征增强
既然在纤维化过程中,也需要KC表型来捕获细菌,而事实情况也是大多数细菌仍能够在肝纤维化过程中被有效捕获(图3K),那么肝脏的适应变化是什么样的呢?作者发现,CCl4处理后,感染葡萄球菌的小鼠存活率仅有微小差异,然而消耗小鼠的巨噬细胞或者KC后感染细菌将导致100%或80%的死亡率(图5A-B)。更有意思的是,CCl4处理后,在侧支血管形成了大量的F4/80+巨噬细胞聚集,偶尔能看到单个巨噬细胞(图5C),这些巨噬细胞集落平均捕获的葡萄球菌在30个左右,并且都表达高水平的CRIg(图5D)。与野生型小鼠相比,CRIg-/-小鼠在CCl4处理8周后也会形成巨噬细胞聚集,但无法捕获细菌(图5G),并且在静脉注射金黄色葡萄球菌MW2后,小鼠肝脏中的菌血症增加,肝脏CFU(colony-forming units)减少(图5H)。侧支血管中的巨噬细胞集落也能够迅速酸化葡萄球菌生物颗粒,其动力学与KC相似,巨噬细胞集落从高流量血管中高效清除细菌的能力因肝脏血流的机械性减少而急剧下降,并在血流恢复正常后迅速恢复(图5I-J)。因此,表达CRIg的巨噬细胞集落的出现将纤维化肝脏的捕获能力从肝窦转移到了侧支静脉。
高分辨率显微镜(图5K)和透射电子显微镜(TEM)(图5L)显示在小鼠纤维化肝脏中发现了多核巨型巨噬细胞,表明在某些情况下这些细胞会融合成巨型细胞,作者将这些命名为“Kupffer细胞样合胞体”。不仅如此,作者在不同病因的肝硬化患者组织中发现了大量的CD68+多核巨细胞集落,这些KC样合胞体也呈CRIg阳性(图5M-O)。
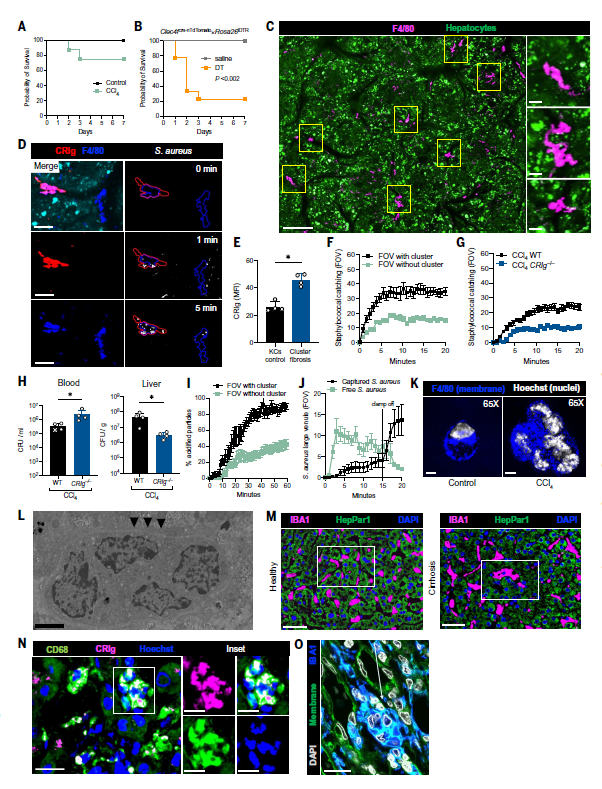 图5 纤维化中出现多核合胞体,Kupffer细胞特征增强
图5 纤维化中出现多核合胞体,Kupffer细胞特征增强
部分相关产品:
| 货号 | 产品名称 | 规格 |
| abs47047620-10ml | Hoechst 33342 | 10ml |
| mihc-DAPI-EA | DAPI染料 | EA |
| abs182389-25T | FITC Mouse anti-Human CD68 Antibody(Y1/82A) | 25T |
05 合胞体具有Kupffer细胞表型,并且来源于骨髓
合胞体除了具有超强的细菌捕获能力、高度表达CRIg之外,还表达TIM-4和CLEC4F,尽管具有KC表型,但约90%的合胞体表达Ms4a3,这也表明合胞体主要来源于单核细胞(图6A-D)。CCl4处理2周时,表达CX3CR1的单核细胞在大血管内广泛募集,并开始表达F4/80,4周时达到巅峰,但在窦内没有募集,而缺乏CX3CR1的KC则位于周围的窦道中,这表明,肝纤维化过程中招募的单核细胞而非更早时期是KC样合胞体的来源。使用PKH标记常驻巨噬细胞,8周的CCl4处理后,窦状KC可被标记,而合胞体不会,这说明窦状KC不是合胞体的来源(图6E-I)。
 图6 合胞体具有Kupffer细胞表型,并且来源于骨髓
图6 合胞体具有Kupffer细胞表型,并且来源于骨髓
部分相关产品:
| 货号 | 产品名称 | 规格 |
| MAB6247-S | Human MS4A3 Antibody | 25ug |
| MAB2784-SP | Mouse CLEC4F/CLECSF13 Antibody | 25ug |
06 Kupffer细胞样合胞体通过CD44和共生微生物被招募
细菌从肠道转移是人类肝硬化的一个特征。相比较对照小鼠,从出生起就接受抗生素治疗的小鼠或者无菌小鼠,在CCl4处理后,合胞体形成显著减少(图7A-B),此外,静脉注射金黄色葡萄球菌也会减少两种小鼠肝脏对细菌的捕获,并增加血液中的细菌数量(图7C-F),经CCl4处理的Myd88-/-小鼠(对细菌感染的敏感性增加)也表现出较少的合胞体形成(图7G)。合胞体从骨髓招募到侧支血管的具体机制是怎样的呢?作者通过分析最近发表的CCl4纤维化模型以及人类肝硬化中单核巨噬细胞的转录组数据集,找到了在细胞融合与粘附过程中上调的一些关键基因:CD9、CD36和CD44,同时CD44是肝脏中多种类型细胞的主要粘附机制。CCl4处理后,CD44-/-小鼠侧支血管中单核细胞数量显著减少,8周后甚至没有KC样合胞体的形成。不仅如此,骨髓派生的CD44而非实质细胞CD44是KC样合胞体形成的必要条件(图7I-L)。与野生型小鼠相比,经CCl4处理后,CD44-/-小鼠肝脏的细菌捕获能力明显降低,纤维化肝脏中的CFU数量减少了三分之一,并且存活率也更低。获得了骨髓派生的KC合胞体的小鼠表现出更强的细菌捕获能力并减少了菌血症(图7M-Q)。更有意思的是,未被细菌感染的野生小鼠和CD44-/-均存活,也就意味着非病理状态下,不涉及KC样合胞体的形成(图7Q)。这些结果证明了:Kupffer细胞样合胞体从骨髓招募到侧支血管依赖于CD44和共生微生物。
 图7 Kupffer细胞样合胞体通过CD44和共生微生物被招募
图7 Kupffer细胞样合胞体通过CD44和共生微生物被招募
部分相关产品:
| 货号 | 产品名称 | 规格 |
| 3578S | CD44 Antibody | 100ul |
07 Kupffer细胞样合胞体依赖于清道夫受体CD36进行细胞粘附和融合
细胞融合与粘附过程中的关键基因除了CD44还有CD9和CD36,作者接下来研究了CD9和CD36是否参与其中。抗CD9阻断抗体对CCl4处理后小鼠合胞体没有影响,CD36-/-小鼠在CCl4处理后未能形成合胞体,但是侧支血管中有大量CRIg+F4/80+细胞,这表明CD36-/-单核细胞被招募,但未能形成合胞体,而是以分散的单个巨噬细胞的形式出现,并且与KC样合胞相比,单个巨噬细胞在络脉中所占的体积要小得多(图8A-C)。作者同样也证明了只有骨髓派生的CD36才是KC样合胞体形成的必要条件(图8D)。经CCl4处理的CD36-/-小鼠的巨噬细胞尽管高度表达CRIg,但是缺乏在较大血管中捕获细菌的能力,小鼠的存活率也较低。同样地,获得了骨髓派生的KC合胞体的小鼠表现出更强的细菌捕获能力以及清除能力(图8E-I),这些结果也证实了Kupffer细胞样合胞体的粘附和融合依赖于CD36。
 图8 Kupffer细胞样合胞体依赖于清道夫受体CD36进行细胞粘附和融合
图8 Kupffer细胞样合胞体依赖于清道夫受体CD36进行细胞粘附和融合
部分相关产品:
| 货号 | 产品名称 | 规格 |
| 74002S | CD36 Antibody | 100ul |
| 98327S | CD9(E8L5J)Rabbit mAb | 100ul |
全文总结
作者的研究结果表明,KC在肝脏处于病理状态下(如肝纤维化)由于自身生态位的改变,会失去巨噬细胞特性及其在肝窦内捕捉细菌的功能。肝脏针对这种变化做出的适应性改变是:招募骨髓中的单核细胞到侧支血管,赋予其KC功能,并且单核细胞聚集形成KC样合胞体,具备更高的细菌捕获及清除能力。具体机制是:肝脏中微生物或者微生物产物的增加以及血管中的高剪切力导致单核细胞被CD44募集,进而形成KC合胞体,同时依赖于CD36进行细胞粘附和融合。
最后告诉大家两个好消息:
·①优宁维 学术中心 【细胞培养】解决方案将在十一月份上线!!!
·②11月6日-12月29日,优宁维联合HyClone、Lonza、Miltenyi、Absin细胞达人创造营活动开启,细胞培养秘籍大师班、争霸赛、爆品直降、满额赠礼,助力您成为一代细胞培养大师!

上海优宁维生物科技股份有限公司
试剂 | 耗材 | 仪器 | 软件 | 定制 | 实验服务 | 供应链
免费热线:4008-168-068
咨询邮箱:info@univ-bio.com
订购商城:www.univ-bio.com
微信公众平台:优宁维抗体专家,欢迎关注!
小优博士(小程序):5大课堂, 让你的科研不再难!









 危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)
危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)  营业执照(三证合一)
营业执照(三证合一)