作为细胞中的“回收站”,溶酶体在维持细胞稳态上发挥着至关重要的作用,小优曾经为大家介绍过溶酶体降解(自噬)与神经退行性疾病的关系,感兴趣的小伙伴们请戳这儿了解。
本文想带大家将焦点从溶酶体降解转移到溶酶体膜上,在溶酶体膜上也存在多种不同类型的蛋白质,包括离子通道、转运体、结构蛋白、酶等, 其中离子通道蛋白由于他们在溶酶体离子动态平衡和跨膜转运、溶酶体膜电位和pH以及细胞营养代谢水平的调控中的重要作用, 受到越来越多的关注。
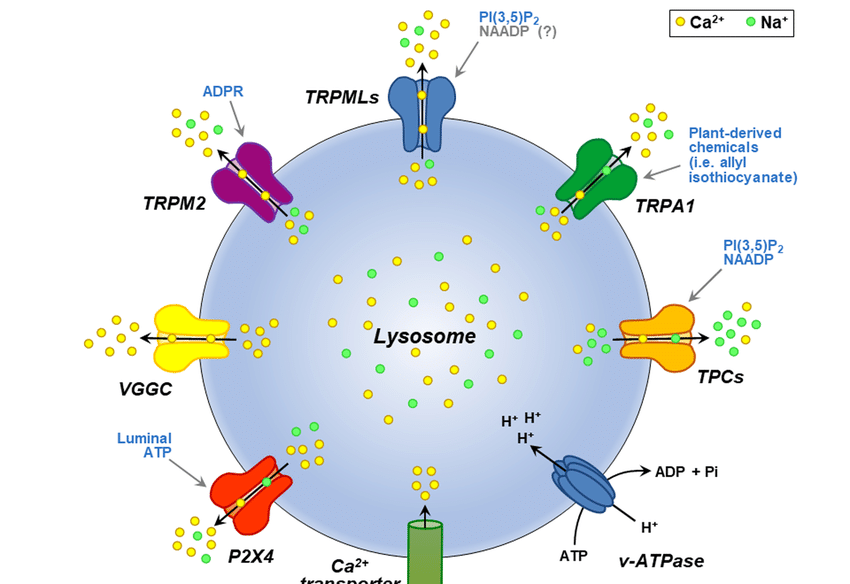
图1.溶酶体膜上的部分相关蛋白质
早在2013年,宾夕法尼亚大学Dejian Ren课题组就在《Cell》上发表了对溶酶体膜表面离子通道TPCN1和TPCN2的相关研究,解释了两个通道如何通过感应细胞外的饥饿环境(如氨基酸缺乏)来增强溶酶体功能,从而更好地利用溶酶体降解来回收生物大分子(如氨基酸),从而维持细胞的存活。除此之外,TMEM175、TRPM1、TRPM2、CLCN、CLCN35等都是溶酶体膜上的热门离子通道/转运体靶标。
近年来,TMEM175对帕金森综合征(PD)的影响越来越受到研究者们的关注。2021年发表于《Nature》期刊,及今年6月发表于《Cell》期刊的两篇文章均对这个与PD相关的溶酶体膜离子通道靶点进行了研究,下面小优就为大家来详细剖析这两篇文章。
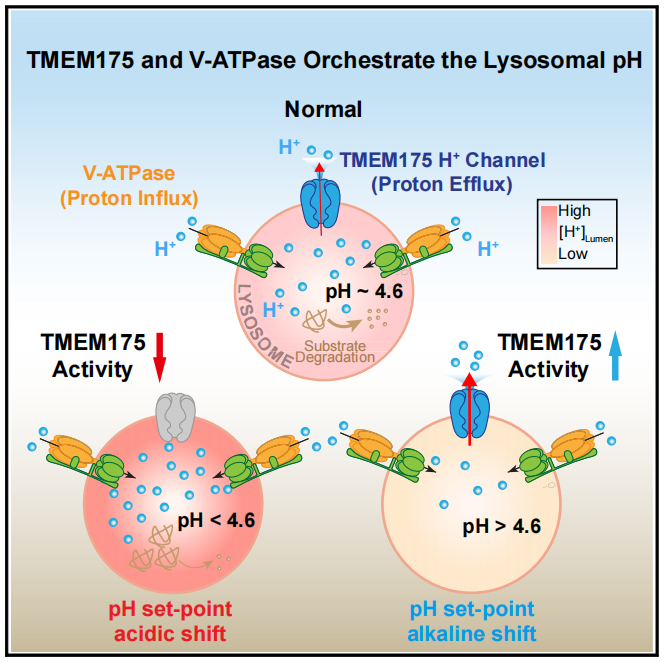
图2. TMEM175是溶酶体在生理酸性条件下氢离子激活通道,通过介导溶酶体氢离子外排来维持稳定细胞内pH的稳定状态
PART ONE: 生长因子通过调控溶酶体钾离子通道参与帕金森病变

该文章揭示了TMEM175会与蛋白激酶protein kinase B (AKT) 形成一种神经元溶酶体复合型钾离子通道,通过感受胞外生长因子,将胞外信号分子与溶酶体的功能联系起来,并且该通道的激活不依赖于激酶的催化活性。
作者首先验证了生长因子(胰岛素、NGF、BDNF)可以激活饥饿状态下小鼠原代海马神经元中的溶酶体钾离子通道。如图三所示,细胞转染TMEM175且饥饿后,钾离子电流就消失了(图3),而通过喂养三种生长因子,消失了的钾离子电流会重新出现。另外,如果在小鼠的原代海马神经元细胞中进行TMEM175基因敲除,钾离子电流也会相应的消失。
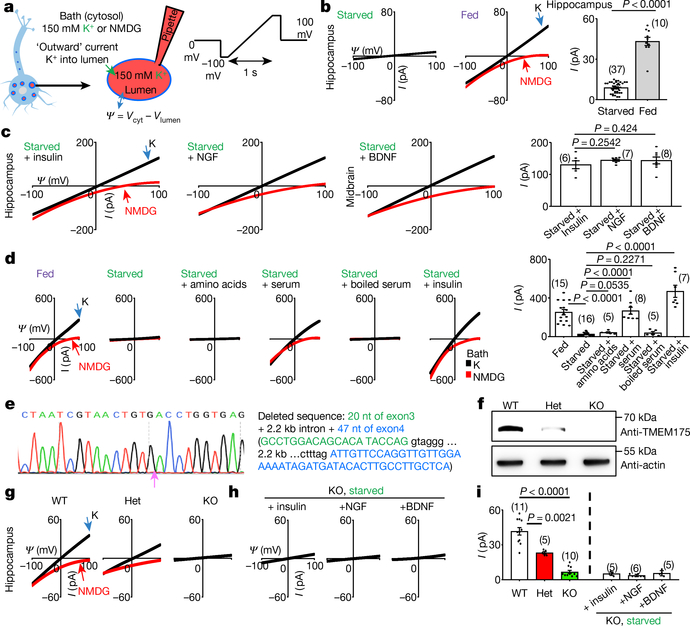
图3.溶酶体钾离子通道可以被生长因子激活
该结果说明了TMEM175会参与通道孔的形成,介导溶酶体钾离子通道。同时这个结果也暗示了生长因子或许可以间接性地通过其受体的靶点,如AKT,来激活TMEM175。因此,作者接下来又对AKT对TMEM175及对溶酶体钾离子通道的激活及调控进行了相关的细胞实验。
如图4和图5,多个细胞实验证明AKT对溶酶体钾离子通道的生成是必要的。且这些实验中的免疫沉淀结果也显示了TMEM175和AKT之间有相互作用,这或许说明了两者之前可以形成一种复合物,而这种复合物对于溶酶体钾离子通道的形成是至关重要的。

图4.AKT可以充分激活TMEM175
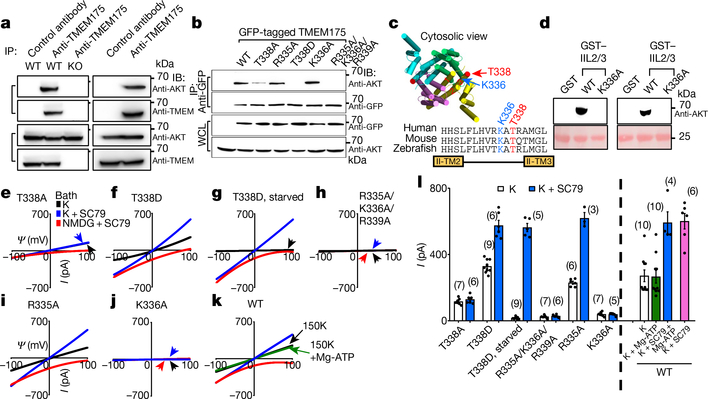
图5.AKT可以通过与溶酶体钾离子通道的相互作用机制激活TMEM175
实验进行到这里已经表明AKT对于TMEM175的激活是必要的,那么是否需要依赖AKT的激酶活性来对TMEM175进行激活呢?答案是否定的,图6就描绘了仅需要AKT构象的改变,就可以使得TMEM175被激活,更多的实验细节请大家参考文献。

图6. AKT的构象改变即可以对TMEM175通道进行激活(GF=growth factors)
接着,作者又研究了TMEM175的两种常见的次要等位基因(minor allele)rs34311866和rs34884217,分别对应的是TMEM175通道的M393T和Q65P两种突变。据研究,前者的变异与PD发病与进展呈正相关,而后者则呈负相关。
如图7(d)的电生理结果可以发现(M393T突变),相较于野生型模型,突变型模型的电流有着显著降低(基础细胞降低43%和sc79激活细胞降低54%)。而对于Q65P突变,野生型样本遭受饥饿3小时后电流消失,突变型样本则在6小时后才会完全消失(图6),说明突变后的模型对胞外生长因子的耐饥饿能力明显更强。
这些结果表明两种突变——M393T和Q65P——类型不同,前者是溶酶体钾离子通道功能丧失型的突变而后者则是功能获得型的突变。同时该文章的补充数据中也显示了,相较于野生型,TMEM基因敲除后的神经元对于神经毒素(MPTP)等恶劣条件的抵御性明显降低,而Q65P的突变模型则可以抵御这种损伤,进一步说明了这类溶酶体钾离子通道对神经具有保护作用。

图7.常见的与帕金森病易感性相关的TMEM175突变(M393T和Q65P)对溶酶体钾离子通道的双向调节作用。
那么该研究中的这种溶酶体钾离子通道如何与帕金森疾病相关呢?Alpha-Synuclein(α-突触核蛋白,α-syn)积累是PD的标志性病症之一。如图8所示,通过免疫荧光及组化实验,作者观察到TMEM175敲除后的小鼠有明显的α-syn累积,TMEM175部分降低的样本(约降低50%)也会加速这种蛋白的聚集。这些结果表明TMEM175的缺失会损害小鼠多巴胺能神经元和其运动能力。

图8.溶酶体钾离子通道的缺乏可导致小鼠致病性α-syn扩散加速、多巴胺能神经元丧失和运动功能受损。
该文章还进行了临床上的验证(图9),结果显示携带有M393T突变的帕金森病人明显具有更低的认知和运动能力(相较于无此突变的病人)。

图9.M393T突变对帕金森病病程的临床研究结果
PART TWO: 与帕金森疾病相关的TMEM175属于溶酶体氢离子通道
今年6月份,该文章的团队发现,在生理酸性的条件下,通过TMEM175的离子主要为氢离子,而非钾离子,并通过一系列的定量分析发现,TMEM175在该条件下对于氢离子的通透性是钾离子的约5万倍之多。
该作者对于这一研究的灵感来源于曾经的一个发现:在对细胞内溶酶体膜直接进行电生理记录时,只要仿照生理条件,溶酶体膜内外存在pH差别(膜外为pH=7.2的中性环境,膜内为pH=4.6的酸性环境),就总是能够记录到从膜内流向膜外的特异性微弱电流。假如将膜内pH调整为更加酸性的3.5,这一信号会更加强烈。
基于此发现,作者做了如下的大胆假设:介导该电流的离子通道即是科学界正在寻找的溶酶体膜上的氢离子通道,与V-ATPase质子泵互相配合,一进一出,共同调节溶酶体的pH平衡。
因此,为了找出这一想要的氢离子通道,作者对一系列可能的溶酶体膜蛋白(除TMEM175外,还有TPC1/TRPML1/CLCN4/CLN8等)进行了逐一的过表达测试(图10)。发现只有在TMEM175过表达的时候,所记录到的电流比其他膜蛋白高出20倍左右。同时,被基因敲除后的样本,即使将pH设定在更低值(3.5)也没有可观察的电流。这些结论表明初步验证了TMEM175就是想要寻找的溶酶体氢离子通道。
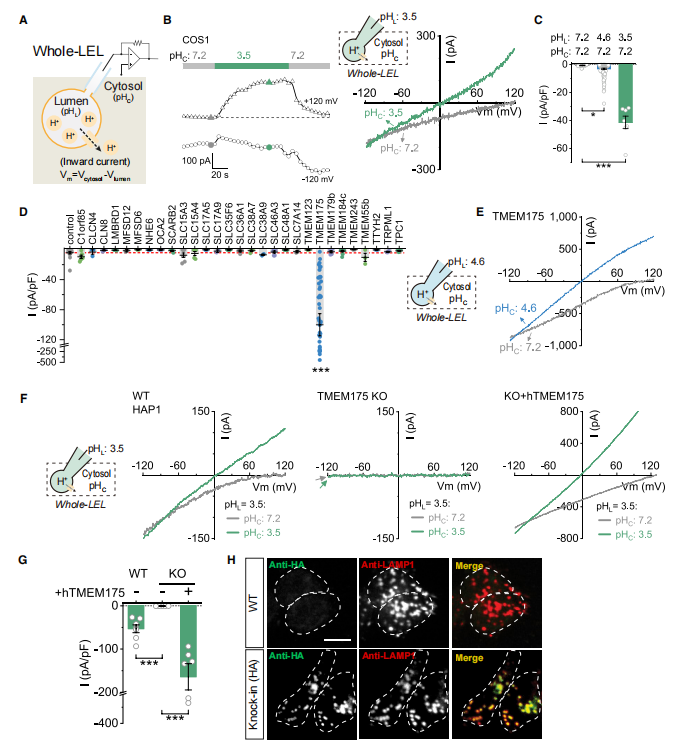
图10. TMEM175对于溶酶体质子激活的质子渗透电流是必要且充分的.
研究进行到这里,发现了与之前研究相悖的结论,即前期研究普遍认为TMEM175是一个钾离子通道,接着该文章对两者的差异又做了进一步的研究。经过仔细对比发现,先前的文献没有针对pH对TMEM175功能的调节作用进行考虑,因此会认为TMEM175主要通透的是钾离子。
因此作者又进行了一系列的将溶酶体内部环境设置在跟接近生理条件pH环境的研究(如图11),发现TMEM175在该pH条件下,具有更强的的氢离子通透性(大约是钾离子的5万倍)。
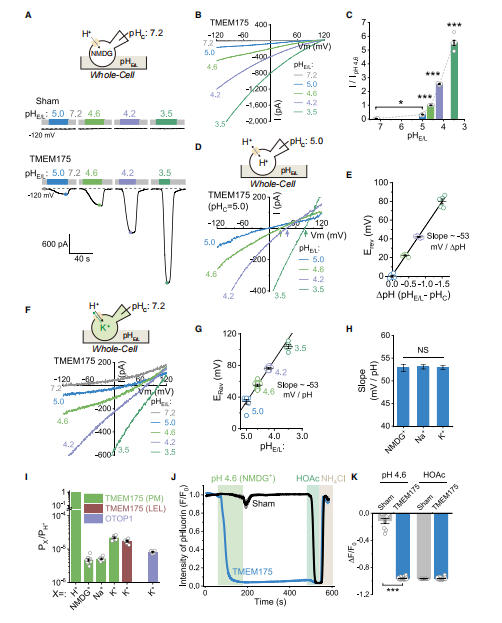
图11.TMEM175通道具有很强的质子通过性
除此之外,该研究还鉴定出小分子化合物DCPIB和ML 67-33也可以激活TMEM175通道。这些化合物不仅能在酸性条件下激活通道的氢离子电流,在中性条件下也同样可以激活钾离子电流(图11)。除此之外,研究还发现脂质分子花生四烯酸(Arachidonic Acid, ArA)是TMEM175通道的内源激活剂,说明脂质信号通路也很可能对TMEM175的活性存在调节作用。
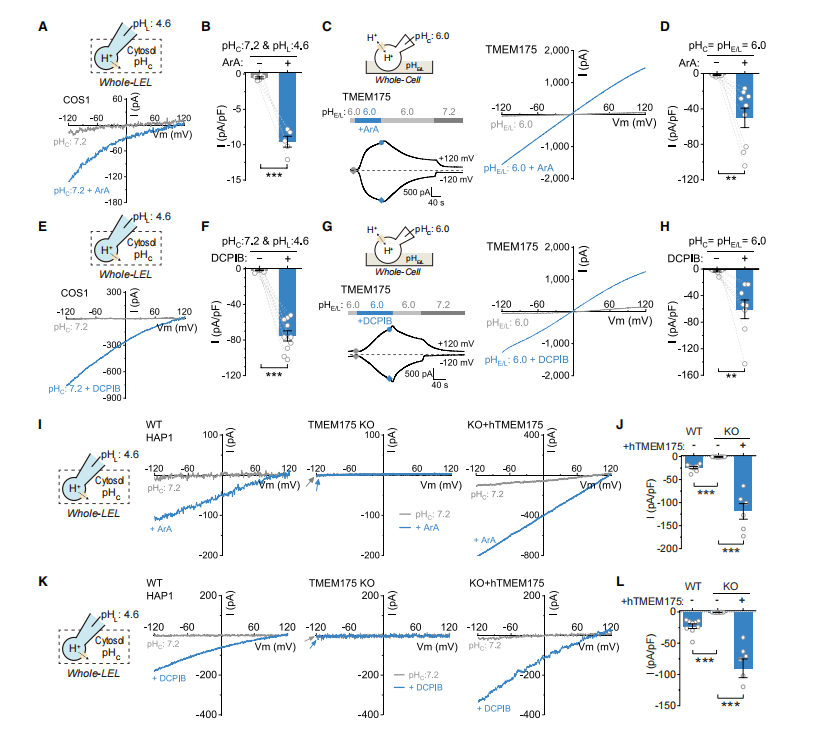
图12.花生四烯酸(ArA)和合成化学物质可以激活TMEM175
在细胞水平上,研究发现进行TMEM175基因敲除后的细胞内溶酶体的pH稳态被破坏,此时的溶酶体处于一种酸性过强的状态,并通过免疫细胞实验发现溶酶体内部的蛋白水解酶Cathepsin B和Cathepsin D的活性也因此受到影响(图13)。

图13. 通过TMEM175的质子渗透是溶酶体pH平衡和有效的蛋白水解降解所必需的
接着研究者从细胞层面衍生至小鼠生物体内,构建了TMEM175基因敲除的动物模型,如图14所示,在小鼠神经元组织中也同样观察到了溶酶体酸性过强、溶酶体降解功能受损的现象。同时,与神经退行性疾病帕金森症致病相关的α-Synuclein(前文提到)聚积现象在TMEM175基因敲除小鼠中也更为显著,从而推测会对PD的病症造成进一步的影响

图14. 小鼠神经元TMEM175的缺乏会导致溶酶体过度酸化,溶酶体水解活性受损,以及小鼠大脑中的α-Synuclein核蛋白的聚积
两篇文章都为PD的研究提供了更广阔的思路,特别是第二篇,揭示了TMEM175是一种新型的氢离子激活的氢离子通道。近年来,研究者在帕金森综合征的病人体内普遍检测到了TMEM175基因的突变,未来,小优预测会有更多的围绕TMEM175调节机制,以及TMEM175如何影响神经退行性模型的精彩研究被陆续发表。
同时,不少研究团队也正在研发用于调控溶酶体离子通道包括TRPML1和TMEM175在内的靶向药物,将来可能用于预防和治疗与溶酶体代谢降解相关的神经退行性疾病,如帕金森症、阿尔茨海默病等。
关于Alomone
Alomone是来自以色列的离子通道抗体专家,每个批次的产品都经过严格的质量控制测试和验证。 抗体产品会通过免疫多肽验证其特异性,其他药理学试剂和重组蛋白则均通过严格的生物检验。
优宁维作为Alomone在中国区的独家授权代理商,建立了中国现货库,为广大客户带去更快的物流,更好的服务。
文中部分相关产品推荐:
抗体
| 货号 | 产品名 |
| sc-9996 | GFP (B-2) |
| sc-7392 | HA-Tag (F-7) |
| 4970 | anti-β-actin |
| 9272 | Akt Antibody |
| 2965 | Phospho-Akt(Thr308)(C31E5E) Rabbit mAb |
| 4691 | Akt(pan)(C67E7) Rabbit mAb |
| MAB2055 | h/m/rAkt Pan MAb (Cl |
| 9271 | Phospho-Akt(Ser473) Antibody |
| 4056 | Phospho-Akt(Thr308)(244F9) Rabbit mAb |
| 9323 | Phospho-GSK-3beta(Ser9)(5B3) Rabbit mAb |
| 9315 | GSK-3beta(27C10) Rabbit mAb |
| 2691 | PRAS40(D23C7)XP Rabbit mAb |
| 2997 | Phospho-PRAS40(Thr246)(C77D7) Rabbit mAb |
| 2284 | Cathepsin D Antibody |
| 7074 | Anti-rabbit IgG, HRP-linked Antibody |
| 7076 | Anti-mouse IgG, HRP-linked Antibody |
| APZ-035 | Anti-Alpha-Synuclein Antibody |
| AGP-008 | Guinea Pig Anti-Alpha-Synuclein Antibody |
| ACC-071 | Anti-TPCN1 Antibody |
| ACC-072 | Anti-TPCN2 |
| sc-365558AC | cathepsin B (H-5) AC |
| sc-377299 | cathepsin D (D-7) |
| HPA057160 | Polyclonal Anti-TMEM175 Antibody |
化合物
| 货号 | 产品名 | Cas No. |
| 111038 | Bafifilomycin-A | 88899-55-2 |
| 10006607 | Arachidonic acid-sodium | 6610-25-9 |
| 90010 | Arachidonic Acid | 506-32-1 |
| 14972 | SC-79 | 305834-79-1 |
| 11593 | MK-2206 | 1032350-13-2 |
| 21388 | ARQ-092 | 1313881-70-7 |
| 10010591 | Wortmannin | 19545-26-7 |
| 1540 | DCPIB | 82749-70-0 |
| 6886 | ML 67-33 | 1443290-89-8 |
| abs814897 | MPTP hydrochloride | 23007-85-4 |
其他试剂/试剂盒
| 货号 | 产品名 | 类型 |
| LS003119 | Papain, Lyophilized | 组织解离试剂 |
| B-250 | Recombinant human BDNF protein | 生长因子 |
| N-100 | Native mouse NGF 2.5S protein (>95%) | 神经生长因子 |
| N-240 | Native mouse NGF 2.5S protein (99%) | 神经生长因子 |
| AK-580 | Parkinson’s Disease Marker Antibody Kit | 帕金森症热门靶点抗体套装盒 |
| AK-530 | Lysosomal Ion Channel Antibody Explorer Kit | 溶酶体离子通道抗体套装盒 |
| LT07-318 | MycoAlert Mycoplasma Detection Kit | 支原体检测盒 |

Nanion全自动膜片钳Port-a-Patch®










 危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)
危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)  营业执照(三证合一)
营业执照(三证合一)