Biacore技术是研究生物分子互作最常用的技术之一。无论是蛋白和蛋白相互作用,蛋白和小分子(或者核酸)相互作用,还是抗原和抗体相互作用,Biacore技术都能手到擒来。Biacore基于表面等离子共振分析原理(SPR)检测互作,具有高分辨率,高灵敏度,无需标记和实时监测的特点。和传统的CO-IP或者CHIP实验相比,Biacore不仅可以检测出待测样品之间是否有特异性的结合,还可以通过数据分析获得分子间的结合速率(Ka),解离速率(Kd)等参数,从而精准的得到亲和力,浓度,动力学,热力学等信息,为生物分子间的相互作用提供准确,可靠和多元化的数据,从而使研究者们对于分子间的互作机制有更深入的了解,并帮助研究者更加高效的进行机制研究,靶点验证,药物研发等。

Biacore具有这么多优越的性能,你是不是也想更加了解Biacore呢?Biacore具体应用的介绍大家可以查看我们之前的文章:分子互作方法之BIAcore!小优也收集了一些Biacore使用者最关心的问题,一起来看看吧。
一、实验设计和芯片选择
1、芯片可以重复使用么?可以重复使用几次?
想要了解这个问题,首先我们要先了解两个概念:共价偶联法和捕获法。
(1)共价偶联法是指配体蛋白通过化学偶联试剂共价地固定于芯片表面,主要是CM系列芯片例如CM5,CM7等等,还有偶联生物素标记配体分子的SA,NA等芯片。和捕获法相比,共价偶联法偶联量高,配体消耗量少,但是偶联在芯片上的配体蛋白无法通过再生去除。
(2)捕获法是指在芯片表面先固定一个与配体蛋白高亲和力结合的捕获分子,然后再通过捕获分子连接配体蛋白,例如NTA,ProteinA,ProteinG芯片等,需要搭配捕获试剂盒使用。芯片再生时会将捕获的配体蛋白连同分析物一同去除,留下捕获分子准备用于下一循环去结合新鲜的配体蛋白。尽管这个方法增加了配体的消耗,但它也避免了再生过程对配体蛋白的损伤,并可以在同一传感芯片上的不同循环间更换不同的配体蛋白。

(3)所以在考虑芯片重复使用的问题时,首先要判断芯片是共价偶联法还是捕获法,如果是共价偶联法,配体蛋白无法通过再生去除,可以随意更换不同的分析物进行其他的实验,偶联了配体蛋白的芯片也可以放在冰箱内保存等待下次使用(具体方法见下方芯片保存),芯片的使用次数主要取决于芯片上已经偶联的配体蛋白是否失活;如果是捕获法,配体蛋白和分析物都可以通过再生去除,可以随意更换不同的配体蛋白和分析物进行其他实验,理论上可以一直重复使用,具体性能需要多次使用后进行测试。
| 共价偶联法 | 捕获法 | |
| 配体蛋白固定方式 | 配体蛋白直接共价偶联在芯片上 | 通过捕获分子偶联在芯片上 |
| 配体定向性 | 无立体定向性 | 有立体定向性 |
| 配体蛋白是否可去除 | 配体蛋白无法去除,分析物可通过再生去除 | 配体蛋白和分析物都可通过再生去除 |
| 配体偶联量 | 较高 | 相对较低 |
| 配体蛋白用量 | 少 | 多 |
| 配体纯度 | 需要较高的配体纯度 | 对配体纯度要求较低 |
| 偶联和再生条件 | 需要摸索 | 参考捕获试剂盒说明书 |
| 芯片价格 | 较低 | 相对较高 |
| 适合于什么实验 | 一个配体对多个分析物实验 | 多个配体对多个分析物实验 |
共价偶联法和捕获法的区别
2、芯片可以偶联几个配体蛋白?
芯片可以偶联几个蛋白主要取决于使用的仪器有几个通道。Biacore T100/T200/S200/3000有4个通道,最多可偶联3种不同样品;Biacore X100/X100 Plus有2个通道,最多偶联1种样品;Biacore 8K有16个通道,最多可偶联8种不同样品;Biacore 1K/1K Plus/1S Plus有6个通道,最多可偶联5种不同样品。
 T200仪器通道示意图
T200仪器通道示意图
以T200为例,在放入芯片后,仪器的微流控系统会把芯片划分为4个独立的通道,这4个通道都可以独立使用。一般会把第一通道作为参比通道,因此还剩下3个通道可以最多偶联3个不同的配体蛋白。
3、His标签蛋白和蛋白互作选择CM5还是NTA芯片?
(1)CM5芯片是共价偶联法芯片,NTA芯片是捕获法芯片,具体的区别可以参考问题1中共价偶联法和捕获法的区别。
(2)简单来说:如果配体蛋白纯度高且量不多,选择CM5芯片;如果配体蛋白纯度不高,可以选择NTA芯片。
(3)如果是做一个配体蛋白和多个分析物的相互作用,首选CM5芯片;如果检测多对蛋白间的相互作用,选择NTA芯片。
其他的需要考虑的点包括:
(4)CM5芯片识别的是蛋白的氨基进行偶联,所以偶联具有不定向性,蛋白的任意氨基位点都可能被占用。而NTA芯片识别的是蛋白的His标签进行偶联,对蛋白本身的位点没有占用。如果担心偶联会影响结合位点,可以考虑用NTA芯片。
(5)如果要检测的分析物也带有His标签,此时不能使用NTA芯片。因为NTA芯片在偶联配体后没有封闭的过程,因此如果分析物也带有His标签,也会被芯片捕获,造成假阳性。
4、蛋白和小分子互作选择CM5芯片还是CM7芯片?
(1)CM7芯片和CM5芯片的偶联化学性质相同,都是通过氨基偶联方式固定蛋白配体。主要区别是CM7芯片表面的葡聚糖羧基化程度高于CM5芯片,所以偶联量是CM5芯片的大约3倍。由于小分子分子量比较小,不易被检测到,使用CM7芯片偶联量高可以提高检测的灵敏度。
具体判断可以参考:大分子/小分子分子量比>200时,选择CM7芯片。
(2)如果您的实验目的是想获得精确的亲和力数值,建议选择固定蛋白,而将小分子作为分析物。考虑到小分子的固定难度、空间位阻以及固定过程对于结合的影响等方面的问题,选择氨基偶联的方式固定蛋白往往是最简单、有效的固定方式。
 CM7芯片偶联量较高
CM7芯片偶联量较高
二、实验操作
1、蛋白和蛋白或蛋白和小分子相互作用对于样品和分析物分别有什么要求?
(1)蛋白作为配体或者分析物时,纯度浓度要求一致: 纯度大于85%;最好有活性;浓度要在0.5mg/ml以上,最好是1-2mg/ml之间的浓度比较合适。
①蛋白作为固定配体:尽可能避开Tris,缓冲液越简单越好,例如常规pbs/hbs。蛋白实际使用量为ug级别,但是考虑具体实验细节,尽量准备100ug左右备用。
②蛋白作为分析物:可以含有Tris,但尽可能避开甘油、蔗糖、咪唑等高折光率物质。
③如果购买商品化蛋白,一般SDS-PADE, WB、Elisa鉴定过的蛋白,做Biacore基本没问题。但不排除蛋白自身的特性,导致结果和预期不符。
(推荐使用脱盐柱PD-10(货号17085101)对配体蛋白进行换液,去除Tris等成分干扰,但需要与蛋白生产厂家确认去除原有Buffer后是否影响活性)
(2)如果小分子不好溶解,可以使用DMSO或者乙醇等有机试剂助溶。Biacore具有溶剂矫正功能,对于需DMSO助溶的小分子样品,同样在running buffer中加入与分析物中相同浓度的DMSO,通过溶剂矫正即可获得真实结果。需要注意乙醇等较易挥发问题,配置试剂要迅速,加样后要及时对样品加盖或者覆膜。
(3)如果分析物的缓冲液中含有海藻糖、甘油等高折光的物质,建议通过脱盐柱置换buffer来置换掉高折光物质。或者考虑稀释倍数在100倍以上,可以先进样试试,当然最好还是置换buffer。
2、Biacore实验如何选择缓冲液?
(1)一般而言常见的缓冲溶液,例如PBS,HEPES等盐溶液都能做Buffer使用。按照经验,HEPES是一种适用于许多蛋白 - 蛋白相互作用的理想缓冲成分,现有商品化的 10 mM HEPES 缓冲液可与 Biacore 系统配套一起使用。
(2)PBS缓冲液通常更适合用于小分子分析物, 这是因为有机缓冲成分如 HEPES 可能会与配体结合并干扰低分子量化合物的准确检测。
(3)激酶(Kinase)实验则推荐使用Tris缓冲液。
(4)推荐在所有缓冲液中包含非离子型表面活性剂(0.05% 表面活性剂P20)以尽量减少蛋白质和其他生物分子在流动系统中发生沉淀的可能。需要注意的是一些应用缓冲液中不能包含表面活性剂,特别是那些涉及脂类囊泡和/或疏水性蛋白的应用。
(5)在缓冲液中添加EDTA 可以去除可能存在于缓冲液中的微量游离二价金属离子。需注意如果使用NTA芯片,样品和缓冲液中不能含有EDTA。
3、蛋白和蛋白相互作用CM5芯片偶联时多种PH的醋酸钠如何选择?
(1)可以使用PH Scouting进行测试,将配体稀释于不同pH的10mM醋酸钠缓冲液中,流经空白的芯片表面,测试静电吸附的效果。此时,配体蛋白并没有真正偶联在芯片上,使用NaOH可以清洗芯片表面,然后做正式配体偶联。
(2)醋酸钠的PH应大于3.5,并小于蛋白的等电点,使蛋白带正电以方便和带有负电的葡聚糖偶联。
(3)在达到预定偶联量时,应尽量选择PH温和的缓冲液进行实验。可以优先使用PH4.5和5.0进行尝试。
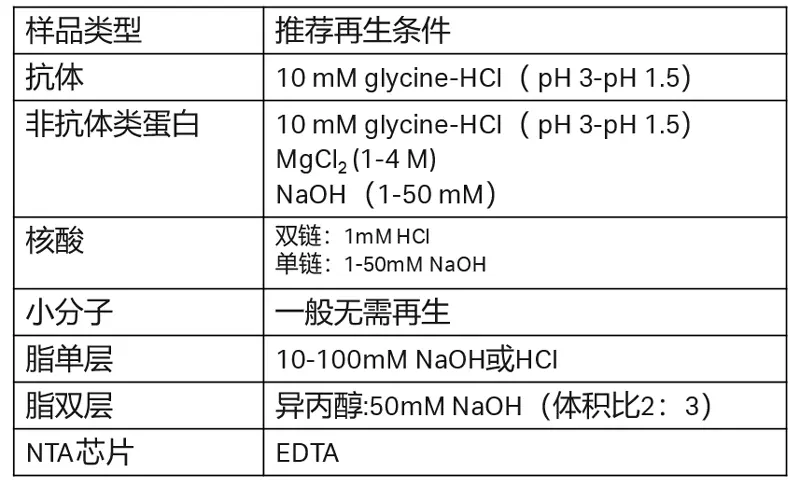
4、再生溶液如何选择?
(1)可使用Regeneration scouting程序,对再生试剂进行测试,选择最合适的再生试剂。
(2)捕获法有对应推荐的再生条件,可参照相对应的捕获试剂盒说明书或如下表格:

(3)常用的再生试剂推荐:
4、分析物浓度梯度如何设置?实验需要设置副孔么?
(1)浓度梯度应设置在0.1-10KD之间,亲和力KD值需在浓度梯度范围内。
(2)常见生物分子间相互作用的亲和力如下范围:

(3)需要设置零浓度样品,并设置一个浓度的样品重复。如果样品充足,建议设置副孔。
三、芯片保存和效期
1、已经偶联配体蛋白的芯片如何保存?
偶联了蛋白的芯片可保存后重复利用,保存时长以配体蛋白活性为准。
(1)湿法保存(长期保存)
移除芯片壳,将中间的一整片芯片放入50mL离心管中,在离心管中加入适量的running buffer,要确保离心管平放时缓冲液没过金膜,可较长时间存放于4℃冰箱中。
(2)半干法保存(短时保存)
推出芯片内片,取大约100ul缓冲液滴在偶联蛋白那面的金膜上,溶液要完全覆盖金膜表面。注意枪头不要接触金膜。将内片推回芯片盒内,水平放入50ml离心管内,密封平放入4℃冰箱中保存。注意过程中不要剧烈晃动,防止液滴脱落。

重复使用时,切记确保芯片各部位干燥后再进行使用,以免损伤仪器。具体操作见下方问题4。
2、芯片保存温度?
参考芯片说明书。一般芯片保存温度为4℃,PEG芯片推荐-20℃保存。
3、芯片的保质期?
可参考包装上的推荐保质期,但由于芯片金膜组件稳定,且未开封芯片均有惰性气体保护,可使用更长时间。
4、芯片从冰箱拿出后应如何处理?
(1)新的芯片室温回温半小时即可使用。
(2)已经有偶联蛋白的芯片从buffer中拿出来可以用水(或去离子水)冲玻璃一面,用无尘纸蘸干(最好不要来回擦);金膜一面不能用水冲,倾斜芯片,水就会聚在一角,用无尘纸折成一个角,将聚集的水吸干净即可(请勿直接接触金膜表面)。
相互作用套餐推荐
1、蛋白和蛋白互作
| 蛋白与蛋白互作 | 29104988 | Series S Sensor Chip CM5-1-pack | 芯片,不同规格选择一个即可 |
| BR100530 | Series S Sensor Chip CM5, 3-pack | ||
| 29149603 | Series S Sensor Chip CM5, 10-pack | ||
| BR100050 | Amine Coupling Kit | 氨基偶联试剂盒,偶联必备 | |
| BR100352 | Acetate 5.5 | 偶联试剂,醋酸钠,用来稀释配体蛋白 |
|
| BR100351 | Acetate 5.0 | ||
| BR100350 | Acetate 4.5 | ||
| BR100349 | Acetate 4.0 | ||
| BR100357 | Glycine 3.0 | 再生试剂,用来去除所有的分析蛋白 |
|
| BR100356 | Glycine 2.5 | ||
| BR100355 | Glycine 2.0 | ||
| BR100354 | Glycine 1.5 | ||
| BR100669 | HBS-EP+ 10 x | 缓冲液,选择一个即可 |
|
| BR100670 | HBS-N 10 x | ||
| BR100671 | HBS-P+ 10 x |
2、蛋白和小分子互作
| 蛋白与小分子互作 | 28953828 | Series S Sensor chip CM7, 1-pack | 芯片,不同规格选择一个即可 |
| 29147020 | Series S Sensor chip CM7, 3-pack | ||
| BR100050 | Amine Coupling Kit | 氨基偶联试剂盒,偶联必备 | |
| BR100352 | Acetate 5.5 | 偶联试剂,醋酸钠,用来稀释配体蛋白 |
|
| BR100351 | Acetate 5.0 | ||
| BR100350 | Acetate 4.5 | ||
| BR100349 | Acetate 4.0 | ||
| BR100357 | Glycine 3.0 | 再生试剂,用来去除所有分析物(小分子也可以不再生) |
|
| BR100356 | Glycine 2.5 | ||
| BR100355 | Glycine 2.0 | ||
| BR100354 | Glycine 1.5 | ||
| BR100672 | PBS 10 x | 缓冲液,选择一个即可 |
|
| 28995084 | PBS-P+ 10X |
3、生物素tag核酸或者小分子与蛋白互作
| 生物素tag核酸或者小分子与蛋白互作 | 不可逆生物素标记捕获 | 29104992 | Series S Sensor Chip SA-1-pack | 芯片,不同规格选择一个即可 |
| BR100531 | Series S Sensor Chip SA, 3-pack | |||
| BR100669 | HBS-EP+ 10 x | 缓冲液,选择一个即可 |
||
| BR100670 | HBS-N 10 x | |||
| BR100671 | HBS-P+ 10 x | |||
| 可逆生物素标记捕获 | 28920234 | Biotin CAPture Kit, Series S | 生物素捕获试剂盒(内含芯片) | |
| BR100669 | HBS-EP+ 10 x | 缓冲液,选择一个即可 |
||
| BR100670 | HBS-N 10 x | |||
| BR100671 | HBS-P+ 10 x |
4、抗体和抗原互作
| 抗体-抗原互作 | 用于直接偶联抗体 | 29127555 | Series S Sensor Chip Protein A 1-p | 芯片,不同规格选择一个即可 |
| 29127556 | Series S Sensor Chip Protein A 3-p | |||
| 29179315 | Series S Sensor Chip Protein G 1-p | |||
| BR100354 | Glycine 1.5 | 再生试剂 | ||
| BR100669 | HBS-EP+ 10 x | 缓冲液 | ||
| human Ab 版 | BR100530 | Series S Sensor Chip CM5, 3-pack | 芯片 | |
| (专用捕获人抗体) | BR100839 | Human Antibody Capture Kit | 人抗捕获试剂盒 | |
| BR100050 | Amine Coupling Kit | 氨基偶联试剂盒 | ||
| BR100669 | HBS-EP+ 10 x | 缓冲液 | ||
| Mouse Ab 版 | BR100530 | Series S Sensor Chip CM5, 3-pack | 芯片 | |
| (专用捕获小鼠抗体) | BR100838 | Mouse Antibody Capture Kit | 鼠抗捕获试剂盒 | |
| BR100050 | Amine Coupling Kit | 氨基偶联试剂盒 | ||
| BR100669 | HBS-EP+ 10 x | 缓冲液 |
5、His标签蛋白互作
| His标签相关互作 | NTA 版 | 28994951 | Series S Sensor Chip NTA, 1-pack | 芯片,不同规格选择一个即可 |
| (芯片表面Ni离子捕获His标签蛋白) | BR100532 | Series S Sensor Chip NTA, 3-pack | ||
| 28995043 | NTA Reagent Kit | 试剂盒 | ||
| BR100670 | HBS-N 10 x | 缓冲液 | ||
| His Ab capture 版 (芯片表面His标签抗体捕获His标签蛋白) |
BR100530 | Series S Sensor Chip CM5, 3-pack | 芯片 | |
| 28995056 | His Capture Kit | His捕获试剂盒 | ||
| BR100050 | Amine Coupling Kit | 氨基偶联试剂盒 | ||
| BR100669 | HBS-EP+ 10 x | 缓冲液 |
6、GST标签蛋白互作
| GST 标签相关互作 |
GST Ab capture 版 (适用蛋白-蛋白互作) |
BR100530 | Series S Sensor Chip CM5, 3-pack | 芯片 |
| BR100050 | Amine Coupling Kit | 氨基偶联试剂盒 | ||
| BR100223 | GST Capture Kit | GST捕获试剂盒 | ||
| BR100669 | HBS-EP+ 10 x | 缓冲液 |
(Biacore X100、X100+、3000 系列仪器把芯片换为Classic系列)









 危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)
危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)  营业执照(三证合一)
营业执照(三证合一)