肿瘤坏死因子超家族(TNFSF)与肿瘤坏死因子受体超家族(TNFR)之间存在着密切的关系。TNFSF成员是一类能够与TNFR成员结合的配体,它们通过这种结合来调节多种细胞功能,包括免疫反应、炎症反应、细胞的增殖、分化和凋亡等。
一、TNFRSF家族的成员具体有哪些,它们各自的功能是什么?
TNFRSF(肿瘤坏死因子受体超家族)是一大类细胞表面受体,它们与TNFSF(肿瘤坏死因子超家族)的配体相互作用,调节多种细胞功能,包括免疫反应、炎症反应、细胞的增殖、分化和凋亡等。目前已知的TNFRSF家族成员包括但不限于以下几种:
1.TNFR1(TNF receptor type 1):含有死亡结构域,能够通过与TNF结合来激活细胞凋亡途径,参与调节免疫反应和细胞死亡。TNFR1(TNF receptor type 1)在几乎所有有核细胞上都有表达,并且含有死亡结构域(DD),能够通过与TNFSF配体结合来激活NF-κB、MAPK等信号通路,诱导炎症反应、细胞增殖、存活或凋亡。TNFR1的激活可以导致细胞凋亡或坏死,这取决于具体的细胞环境和信号复合体的形成。
2.TNFR2(TNF receptor type 2):TNFR2(TNF receptor type 2)的表达相对受限,主要在免疫细胞如T细胞和巨噬细胞以及某些非免疫细胞如内皮细胞和神经细胞中表达。TNFR2不含有死亡结构域,但能够通过TRAF结构域激活NF-κB、MAPKs、AKT等信号通路,参与组织再生、细胞增殖等稳态维持过程。
在炎症性疾病中,TNFR1和TNFR2的作用可能相反;TNFR1通常与炎症和细胞死亡相关,而TNFR2则与组织修复和免疫调节相关。这种差异导致了对TNFR1和TNFR2的靶向治疗策略的开发,旨在选择性地调节它们的信号传导,以治疗特定的疾病。
3.CD40:在B淋巴细胞的激活和免疫应答中发挥关键作用,与多种自身免疫性疾病的发生和发展密切相关。
4.Fas(TNFRSF6):通过诱导细胞凋亡参与免疫耐受的维持。
5.TRAIL-R(TNF-related apoptosis-inducing ligand receptor):包括TRAIL-R1(DR4)和TRAIL-R2(DR5),能够诱导细胞凋亡,是研究肿瘤治疗的潜在靶点。
6.TNFRSF19(TROY):在神经系统发育和干细胞干性维持中发挥重要生理功能,在不同肿瘤中发挥截然相反的促癌或抑癌功能,其功能与肿瘤的组织来源密切相关。
7.TNFRSF11B(OPG):具有骨代谢调节功能,可以抑制骨的破坏和吸收,也被称为骨保护素。
8.TNFRSF9(CD137):是重要的激活型免疫检查点分子,可能成为肿瘤治疗的潜在靶点。
9.TNFRSF11A(RANK):与TNFRSF11B(OPG)一起参与骨代谢的调节。
这些成员根据其细胞内区域是否包含死亡结构域(DD)可以分为死亡受体和非死亡受体两大类。死亡受体包含DD,能够诱导细胞凋亡。非死亡受体缺乏DD,但通常包含TRAF结合序列,能够招募TRAF家族蛋白,参与细胞存活、增殖和细胞因子分泌。此外,TNFRSF成员还可能作为诱饵蛋白,参与细胞内信号通路的负反馈调节。
二、TNFSF家族成员有哪些?它们各自功能是什么?
TNFSF(肿瘤坏死因子超家族)是一组具有广泛生物学功能的细胞因子,它们在免疫调节、细胞凋亡、炎症反应、细胞增殖和分化等方面发挥重要作用。
1.TNF-α (TNFSF2):主要参与免疫调节、炎症反应和细胞凋亡。
2.LT-α (TNFSF3):与TNF-α相似,参与免疫调节和炎症反应,也被称为肿瘤坏死因子β(TNF-β)。
3.CD40L (TNFSF5):与CD40结合,在B淋巴细胞的激活和免疫应答中发挥关键作用。
4.TRAIL (TNFSF10):能够诱导肿瘤细胞凋亡,而对正常细胞影响较小,是肿瘤治疗的潜在靶点。
5.RANKL (TNFSF11):参与骨代谢的调节,与骨质疏松症的发生有关。
6.TWEAK (TNFSF12):参与组织重塑和纤维化过程。
7.BAFF (TNFSF13B):参与B淋巴细胞的成熟和存活。
8.LIGHT (TNFSF14):与免疫细胞的增殖和分化有关。
9.TL1A (TNFSF15):一种促炎分子,参与自身免疫性疾病的发生。
10.FasL (TNFSF6):诱导细胞凋亡,参与免疫耐受的维持。
这些只是TNFSF家族的一部分成员,每一种成员都有其特定的生物学功能和作用机制。例如,TNF-α和LT-α能够与TNFR1和TNFR2结合并介导相似的细胞信号转导,参与免疫调节、炎症反应和细胞凋亡等生物学过程。而CD40L则通过与CD40受体结合,在B淋巴细胞的激活和免疫应答中发挥关键作用。TRAIL则因其能够选择性地诱导肿瘤细胞凋亡而成为肿瘤治疗研究的热点。
三、TNFSF与TNFRSF结合相关检测
1、TNFSF与TNFRSF蛋白
TNF-α Protein, Human和TNFR-1/CD120a Protein, Human结合验证数据:
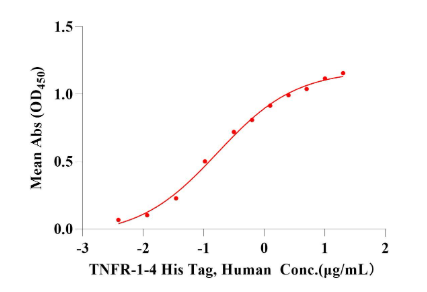 图:TNF-α Protein, Human和TNFR-1/CD120a Protein, Human。EC50:0.167μg/ml.
图:TNF-α Protein, Human和TNFR-1/CD120a Protein, Human。EC50:0.167μg/ml.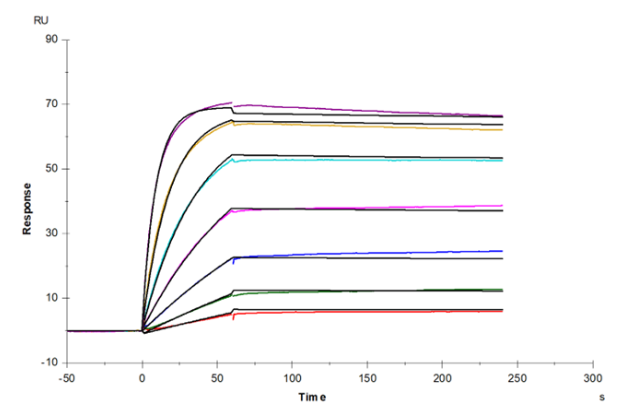
图:Anti-His antibody Immobilized on CM5 Chip captured TNFR-1/CD120a His Tag, Human (Cat. No. UA040028), can bind TNF-α, Human (Cat. No. UA040005) with an affinity constant of 0.106nM as determined in SPR assay.
2、TNFSF与TNFRSF抗体
Anti-TNF-α Monoclonal Antibody生物活性验证:
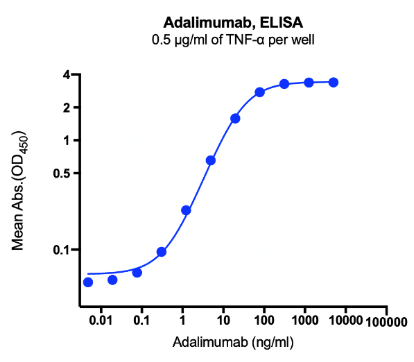 图:Immobilized human TNF-α at 0.5 μg/ml (50μL/well) can bind to Adalimumab with a linear range of 0.305 ng/ml to 5 μg/ml.
图:Immobilized human TNF-α at 0.5 μg/ml (50μL/well) can bind to Adalimumab with a linear range of 0.305 ng/ml to 5 μg/ml.
3、TNFSF与TNFRSF TR-FRET结合试剂盒
1) TNF-a & TNFR1 Binding
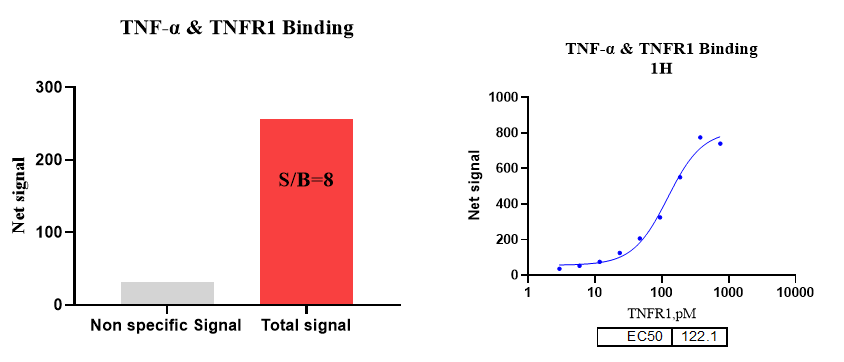
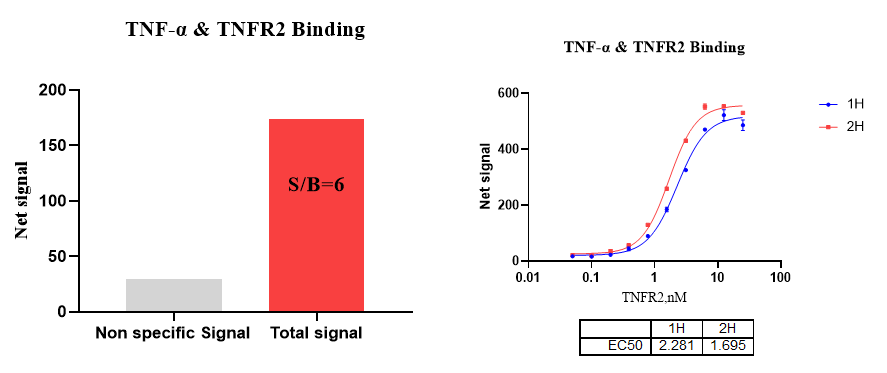
2) TNF-a & TNFR2 Binding
四、信号通路检测
TNFSF与TNFRSF参与NF-κB、MAPKs、AKT等信号通路,
THUNDER TR-FRET时间分辨荧光共振能量转移是一种基于荧光共振能量转移(FRET,Fluorescence Resonance Energy Transfer)和时间分辨荧光(TRF, Time-Resolved Fluorescence)的技术,采用夹心法,检测胞内蛋白磷酸化水平。
Phospho-NF-κB检测技术原理及数据展示如下:
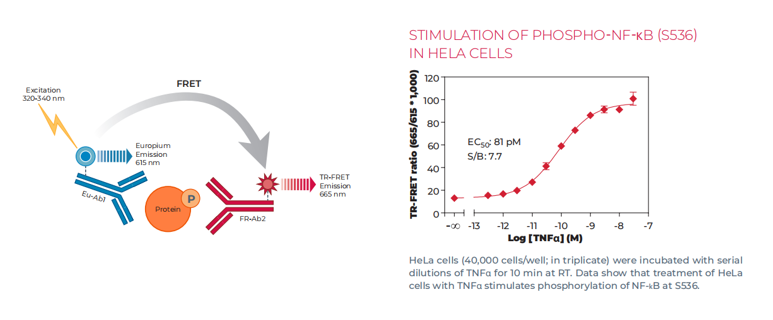 图:THUNDER TR-FRET检测原理示意图及数据展示
图:THUNDER TR-FRET检测原理示意图及数据展示
Tips:诺华(Novartis)在ISAC—免疫刺激抗体偶联物NJH395项目中,使用Thunder技术检测Phospho-NF-κB水平。用MIM697处理1h,检测THP-1细胞内的磷酸化NF-kB。使用TC处理的96孔板培养THP-1细胞,200ml培养基中加入125ng/mL PMA,37℃,5%二氧化碳孵育48h,生成贴壁细胞。去除培养基,用200 mL不含PMA的培养基替换,37℃,5%二氧化碳下静置24小时。去除培养基,在细胞中加入50 mL的培养基。MIM697用培养基连续稀释,在试验孔中加入50 mL。在37℃,5%二氧化碳下孵育1h。按照贴壁细胞二板检测方案进行检测。裂解液转移到384孔板,与检测抗体在4℃下孵育过夜后进行检测。(方法可提供参考)
Phospho-AKT检测数据展示如下:
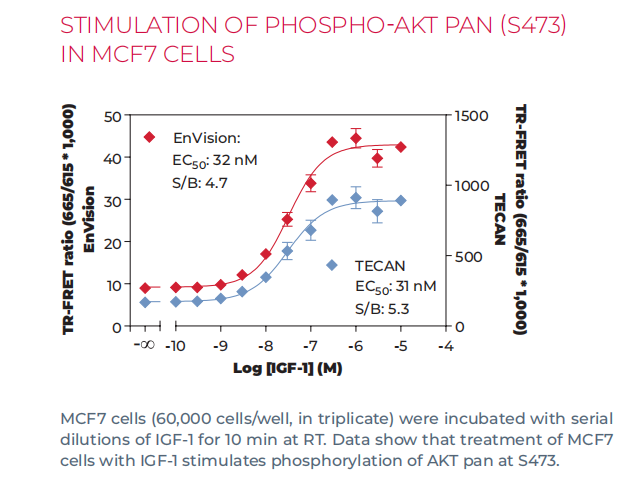 图:THUNDER TR-FRET Phospho-AKT数据展示
图:THUNDER TR-FRET Phospho-AKT数据展示
相关产品推荐:
| 磷酸化蛋白检测 | ||
| 品名 | 货号 | 规格 |
| THUNDER™ Phospho-NF-kB (S536) Kit | KIT-NFKBP-500 | 500 pionts |
| Phospho-AKT pan (S473) | KIT-AKTS473P-500 | 500 pionts |
| Phospho-AKT pan (T308) | KIT-AKTT308P-500 | 500 pionts |
| Total AKT pan | KIT-AKTT-500 | 500 pionts |
| Phospho-p53 (S15) | KIT-P53P-500 | 500 pionts |
| Phospho-p38αβγ MAPK (T180/Y182) | KIT-P38P-500 | 500 pionts |
| Phospho-p38α MAPK (T180/Y182) | KIT-P38AP-500 | 500 pionts |









 危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)
危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)  营业执照(三证合一)
营业执照(三证合一)