研究概述
胰腺导管腺癌(PDAC)是极具侵袭性和致命性的恶性肿瘤之一,尽管治疗策略不断进步,其预后仍然较差。癌相关成纤维细胞(CAFs)作为肿瘤间质中的主要细胞类型,在PDAC的演进过程中起着关键作用,它们能够表现出可塑性,并具有肿瘤促进、肿瘤抑制或稳态功能。然而,CAFs如何促进PDAC的化疗耐药性的具体机制尚未完全明确。近日,广东省人民医院的研究人员在Molecular Cancer杂志上发表了一项重要研究,揭示了circFARP1在CAF中促进吉西他滨(GEM)耐药性的关键作用,为PDAC的治疗提供了新的见解。

研究内容
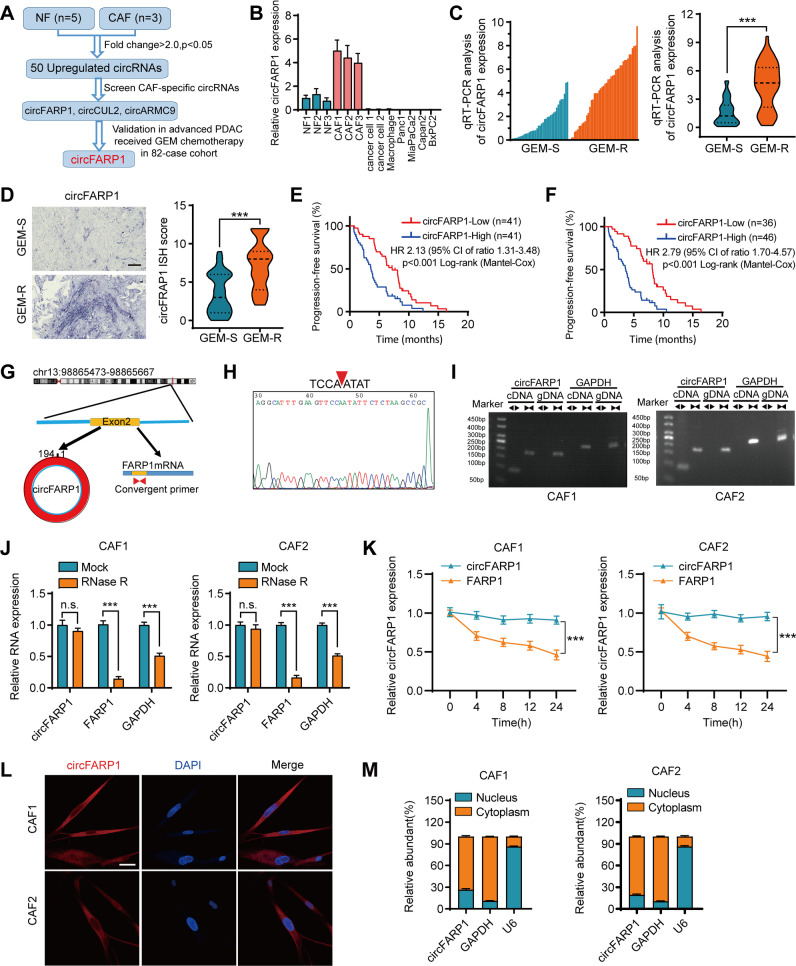
研究者首先利用环状RNA测序和实时荧光定量PCR(qRT-PCR)技术筛选CAF特异性的环状RNA。在众多候选分子中,circFARP1被确定为一个与PDAC吉西他滨耐药性高度相关的CAF特异性环状RNA。随后的研究进一步探讨了circFARP1表达对体外和体内肿瘤细胞吉西他滨耐药性的影响。研究者发现,沉默circFARP1可以降低CAFs通过白血病抑制因子(LIF)诱导肿瘤细胞干细胞特性和吉西他滨耐药的能力,而过表达circFARP1则能够增强这种能力。
为了深入探究circFARP1的作用机制,研究者利用了一系列分子生物学技术,包括RNA测序(RNA-seq)、RNA拖拽(RNA pulldown)、RNA免疫沉淀和荧光素酶报告基因检测。这些实验揭示了circFARP1通过直接与小窝蛋白1(CAV1)结合,并阻断CAV1与E3泛素蛋白连接酶锌和环指1(ZNRF1)的相互作用,从而抑制CAV1的降解,进而增强LIF的分泌。此外,circFARP1还能够作为分子海绵吸附microRNA-660-3p(miR-660-3p),上调LIF的表达水平。

值得注意的是,研究者还发现circFARP1的高表达与PDAC患者血清中LIF水平的升高以及患者的低生存率呈正相关。这一发现进一步支持了circFARP1在CAF介导的吉西他滨耐药性中的关键作用。为了验证这一结论,研究者还利用患者来源的异种移植模型进行了实验,发现降低circFARP1水平和中和LIF能够显著抑制PDAC的生长和吉西他滨耐药性。
研究综述
综上所述,这项研究揭示了circFARP1在CAF中高表达,并通过增强LIF的分泌和表达,诱导胰腺细胞中的STAT3信号通路,从而促进PDAC的吉西他滨耐药性。这是首个揭示环状RNA介导的LIF旁分泌信号的生物学报告,为理解CAF在PDAC化疗耐药性中的作用提供了新的视角。此外,研究者还提示,针对肿瘤微环境(TME)中的circFARP1/CAV1/miR-660-3p/LIF轴制定合理策略,以克服胰腺癌患者的吉西他滨耐药,可能是未来PDAC治疗的重要方向。这一发现不仅加深了我们对PDAC化疗耐药机制的理解,也为开发新的治疗策略提供了潜在的靶点。
| 名称 | 货号 | 规格 |
| Ubiquitin (P4D1) Mouse mAb | 3936S | 100ul |
| Stat3 (124H6) Mouse mAb | 9139S | 100ul |
| HU LIF COATED ELISA | BMS242 | 96Tests |
| DYNABEADS PROTEIN A | 10002D | 5ML |










 危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)
危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)  营业执照(三证合一)
营业执照(三证合一)