IPS诱导脑类器官培养分为两大阶段:多能干诱导神经干细胞分化,神经干诱导形成脑类器官。
人多能干细胞的培养方法
一、实验准备:
1、人多能干细胞培养基配制
(1) 2-8℃解冻 hPSC Medium Supplement,融化后上下晃动混匀,按实际用量进行分装,立即使用或储存于-20~-80℃,避免反复冻融;
(2)按 1:50 的比例将 hPSC Medium Supplement(10mL)加入到 hPSC Medium Basal Medium(500mL)中,混合均匀即成为人多能干细胞培养基(abs9403)。
注意:混匀后的人多能干细胞培养基可在2-8℃ 稳定储存 2-3 周,不建议使用配制已超过 3 周的人多能干细胞培养基。
(3) 实验试剂平衡:人多能干细胞培养基实验前放置室温避光平衡;PBS,消化液等 37℃加热。
注意:培养基中含有因子,不要37℃水浴加热。
二、操作方法(以下步骤皆应在无菌条件下操作)
hPSC 细胞复苏:
1、实验操作步骤:
1.1、基质胶包被培养板:取出 6 孔板/12 孔板,每孔内加入 1 mL/0.5 mL 即用型基质胶(abs9410),轻轻晃动 6 孔板/12 孔板使基质胶完全覆盖皿底,置于 37℃培养箱中孵育 1h~2h,实验前拿出并置于超净工作台/生物安全柜中室温下平衡 20min。如果暂时不用,可用 Parafilm 封口后 2-8℃ 储存,并于 1 周内使用。
注意:
①一支冻存的干细胞的数量在 1×106cells/mL 左右,对应 6 孔板 1 孔;
②即用型基质胶对温度敏感,即用即拿,用完后立即放回 4℃冰箱保存,且勿用手直接触碰基质胶液面所及的瓶身,影响基质胶质量。
1.2、先将 2~3mL 的干细胞培养基加入 15mL 离心管中备用。
1.3、解冻:将从液氮中取出的冻存管快速浸入 37℃温水中,快速摇动,使其在 1~2min 内快速解冻;
注意:细胞从液氮中拿出的速度要快,尽量减少其暴露在室温中的时间。
1.4、离心:冻存管中的冻存液解冻后,将其逐滴加入含有干细胞培养基的 15mL 离心管中,将 15mL 离心管置于低速离心机中配比平衡后,1000rpm 离心 3min;
1.5、重悬:离心后弃上清加 1mL 人多能干细胞培养基对干细胞沉淀进行吹吸混匀,吹吸 3~5 次左右。
1.6、接种:吹吸均匀后,将已经平衡好的即用型基质胶弃掉,将吹打均匀的干细胞悬液加入到已经包被好的 6 孔板中,并补全每孔 2mL 培养体系。
1.7、培养:接种后的 6 孔板可以置于倒置相差显微镜下观察接种的干细胞密度以及细胞团块大小,呈 4个细胞以上的团块较合格,水平十字轻轻晃动 6 孔板/12 孔板使细胞均匀分布。并置于 37℃,5%CO2 的恒温培养箱培养,第 2 天观察细胞贴壁情况;
1.8、换液:从复苏的时间开始每 24h 换液一次。
注意:因培养基中活性成分只足够维持一天,所以每 24h 应及时更换新鲜培养基。
 多能干细胞(PSCs)集落
多能干细胞(PSCs)集落
hPSC 细胞传代:
2、实验具体操作步骤:
2.1、清洗:吸掉原有培养基,贴壁缓慢加入 1 mL PBS 缓冲液并轻轻晃动,然后沿培养皿边缘吸去 PBS缓冲液;
2.2、消化:在 6 孔板中加入 2mL/孔人多能干细胞消化液(abs9409)使之覆盖皿底,并置于 37℃培养箱中 2~5 min;
注意:消化时间依据干细胞生长密度,消化时间略有不同,根据经验一般建议时间 2-5min。消化过程中可以拿到倒置显微镜下观察细胞消化情况,若在显微镜下观察到大部分克隆边缘以及克隆内部细胞间出现间隙,即可吸掉消化液终止消化。
2.3、吹打:吸掉消化液后,加入 2mL 人多能干细胞培养基,用移液枪扇形吹打培养皿底,轻柔吹打 3~5次,使皿底干细胞集落脱落,并将其并转移到 15mL 离心管中;
注意:吹吸皿底细胞的力度要轻柔,吹打脱落和吹吸混匀的次数在 3~5 次为宜,尽量避免形成单细胞。如有少量细胞无法从皿底脱落,属于正常现象。如有大量细胞无法从皿底脱落,需延长消化时间。
2.4、离心:1000rpm 离心 3min,弃上清;
2.5、接种:用干细胞培养基吹打细胞 5-10 次,吸掉包被培养板中的基质胶,并将细胞悬液加入到培养板中,且补全每孔 2mL 的培养体系。
注意:吹打细胞要温柔,并且吹打次数不要超过 10 次。
2.6、换液:从传代的时间开始每 24h 换液一次。
注意:因培养基中活性成分只足够维持一天,所以每 24h 应及时更换新鲜培养基。
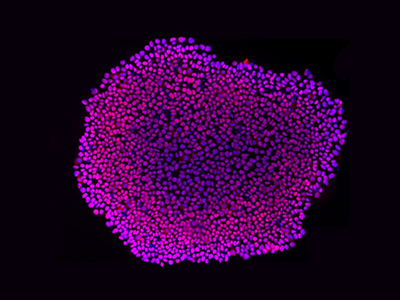
多能干细胞(PSCs)集落染色图
hPSC 细胞冻存
3、实验具体操作步骤:
3.1、清洗:同 2.1;
3.2、消化:同 2.2;
3.3、吹打:同 2.3;
3.4、离心:同 2.4;
3.5、重悬:离心后弃上清,加入 2 mL ES/iPS细胞冻存液(abs9412)对干细胞沉淀进行吹吸混匀,吹吸 3~5 次后,将其加入到冻存管中;
注意:冻存液即用即拿,及时放回 4℃冰箱。
3.6、记录:在冻存管上标记冻存细胞种类、时间、操作者及细胞批次。
3.7、-80℃冰箱冻存:冻存管置于-80℃冰箱过夜。
注意:冻存管放置于-80℃冰箱时,要将冻存管直立放置,切忌冻存管斜放或横放。
3.8、液氮冻存:24 小时后将-80℃冰箱中的细胞转移至液氮中长期冻存。
人多能干细胞诱导神经干细胞分化方法
诱导培养基准备
1、将冷冻的PSC 补充液在2°C至8°C下解冻过夜,或在37°C水浴中快速解冻约5分钟。
2、解冻后的补充液可分装成多个相同的等份,并在-5°C至-20°C保存,以制备较小体积的完整培养基。不要重新冷冻解冻。
3、将小瓶轻轻倒置几次,混合解冻后的补充液。
4、从瓶中取出20mL PSC补充液,转移到PSC培养基瓶中。旋转瓶子混合,即得 500mL人多功能干细胞(PSC) 诱导神经干培养基(abs9822),简称诱导培养基。
5、诱导培养基可在2°C至8°C保存2周。使用前,在37°C 水浴中预热当天所需量的完整培养基5-10分钟。
PSC细胞准备
1、按照人多能干细胞的培养方法—hPSC 细胞复苏步骤—1.1-1.8复苏PSCs。
3、当PSCs达到70-80%的融合度时,去除任何分化和部分分化的克隆。
4、对PSCs进行传代操作,按照人多能干细胞的培养方法—hPSC 细胞传代步骤—2.1-2.4传代
5、从新包被的6孔板中吸除包被液,并在每孔中加入2.5 mL 诱导培养基。
6、轻轻摇动含有诱导细胞悬液的离心管,将PSC以每孔2.5×105 - 3×105的细胞加入包被的6孔板中。例如,如果PSC 悬液中的细胞团浓度为1×106个/mL,则在每孔中加入0.25-0.3 mL的诱导培养基。
7、快速前后左右移动培养皿,使细胞分散在培养皿表面,并将其轻轻置于37°C、5% CO2的培养箱中。
注意:传代PSCs 时,细胞应以小团块的形式接种,而不是单个细胞悬液。避免将PSCs作为单个细胞进行接种,因为这会导致细胞死亡增加。
注意:您可以在分裂时将10 μM ROCK抑制剂Y27632加入PSC培养基中过夜,以防止细胞死亡。
神经诱导
1、预热诱导培养基至室温。
2、在神经诱导的第0天(PSC传代后约24小时),PSC应达到15-25%的融合度。抽吸废培养基,在6孔板的每孔中加入2.5 mL预热好的诱导培养基。将培养皿放入37°C、5% CO2的培养箱中。
3、在神经诱导的第2天,细胞集落的形态应该是一致的。标记所有非神经分化克隆,如果有的话,用巴斯德玻璃移液管或移液管尖端去除这些不需要的克隆。抽吸废培养基,在6孔板的每孔中加入2.5 mL预热好的诱导培养基。将培养皿放回培养箱。
4、在神经诱导的第4天,细胞将达到融合。任何非神经分化的克隆都应标记并移除。从每孔中抽吸废培养基,每孔用5ml 预热的诱导培养基代替,将培养皿放回培养箱。
5、在神经诱导的第6天,细胞应接近最大融合。去除任何非神经分化克隆,在每个孔中加入5mL预热的诱导培养基。将培养皿放回培养箱。
注:在神经诱导的第4~7天,如果细胞的颜色变为褐色, 并且有许多漂浮细胞,说明PSCs的起始密度过高。在这种情况下,每天更换培养基,每孔加5mL 诱导培养基。
6、在神经诱导的第7天,NSCs (P0)已经准备好收获和扩增传代。
人神经干细胞培养方法
准备神经干细胞(NSC)扩增完全培养基
1、NSC 完全培养基需要补充NSC 补充剂、L-丙氨酰-谷氨酰胺。
2、在无菌环境中,依次将20mLNSC补充剂和5ml 200mML-丙氨酰-谷氨酰胺(abs9295)(2mM终浓度)加入到含有480mL NSC 培养基中,此时即得神经干细胞(NSC)扩增完全培养基(abs9821)。
4、(可选)在培养基中加入10mL/L的抗生素(青霉素-链霉素)溶液。
注意:
1、在所有成分的有效期限内,在2°C至8°C的黑暗环境中储存,可稳定长达4周。
2、可选择添加200μM抗坏血酸,特别是悬浮培养。
包被孔板
1、基质胶包被培养板:取出 6 孔板/12 孔板,每孔内加入 1 mL/0.5 mL 即用型基质胶(abs9410),轻轻晃动 6 孔板/12 孔板使基质胶完全覆盖皿底,置于 37℃培养箱中孵育 1h~2h,实验前拿出并置于超净工作台/生物安全柜中室温下平衡 20min。如果暂时不用,可用 Parafilm 封口后 2-8℃ 储存,并于 1 周内使用。
2、在使用前,将已经平衡好的即用型基质胶弃掉,然后加入预热的完全NSC培养基。
NSC传代
1、当细胞密度达到90-100%的融合度时,丢弃培养瓶中的培养基。
2、用5mL不含钙和镁的预温DPBS洗涤细胞,然后吸弃溶液。
3、在每个培养瓶中加入1.0mL预热的人多能干细胞消化液(abs9409),然后在室温下孵育2-5分钟。在孵育前确保完全覆盖细胞。
4、用倒置显微镜观察细胞是否脱离。如有必要,轻拍培养瓶以促进细胞脱离。
5、轻轻上下移液,使团块分散到单个细胞悬液中。
6、加入9mL预热好的NSC 完全培养基停止细胞解离反应,然后将细胞悬液转移到无菌离心管中。
7、200×g离心4分钟。
8、丢弃上清,然后用适量NSC 完全培养基重悬细胞沉淀。
9、用自动细胞计数器测定总活细胞密度。
10、从每个覆盖层培养瓶中除去覆盖层溶液,然后加入5mL预热的NSC完全培养基,添加Y27632(终浓度10μM)。
11、在每个培养瓶中加入5×104细胞/cm2(例如,1.25×106细胞/T-25培养瓶),然后混合或旋转细胞悬液以确保均匀分布。
12、于37°C,5%CO2的潮湿环境中孵育。
注:为了获得最佳性能和细胞生长,每2-3天更换一次培养基,用新鲜的预热的NSC完全培养基。
NSC冻存
1、准备干细胞冻存液(abs9412)。
2、按照“NSC传代”中的步骤1至步骤7收集细胞进行冷冻保存。
3、在离心过程中,计算细胞密度为2×106个活细胞/mL所需的最终体积。
注:接下来的步骤需要半体积的室温NSC培养基和半体积的冻存液。
4、丢弃上清,然后用NSC 完全培养基重悬细胞。
5、加入等量的冻存液,使终浓度为10%DMSO。
6、立即将细胞悬液等分放入冻存瓶中(1mL/瓶)。
7、按照标准程序(每分钟降低1°C)在自动或手动控制速率的冷冻设备中实现低温保存。
8、将冷冻细胞转移到液氮中。
NSC复苏
1、在37°C水浴中迅速(<2分钟)解冻细胞。
2、用移液管将冻存液全部移入无菌的15mL离心管中。
3、小心滴加(每秒1滴),加入4mL预热好NSC 完全培养基,然后轻轻旋转离心管混合。
4、继续添加预热的 NSC 完全培养基至10mL。
5、200×g离心4分钟,确认细胞沉淀,丢弃上清。
6、加入5mL预热好NSC完全培养基重悬细胞沉淀,然后添加Y27632(终浓度10μM),再将离心管的全部内容物转移到包被的组织培养瓶中。
7、于37°C,5%CO2的潮湿环境中孵育。
8、复苏后24小时用新鲜的预热过的NSC 完全培养基替换培养基。
注:为了恢复在NSC 中生长的细胞,我们建议在初始传代时以≥1×105个细胞/cm2的密度接种细胞。
人神经干细胞诱导形成脑类器官
原代
一、准备工作
1、仪器设备
CO2 培养箱、双人单面超净台、倒置显微镜、台式冷冻离心机、水浴锅(abs72023)或水浴摇床,医用冰箱、-80℃冰箱、移液器(一套)。
2.试剂耗材(以肠癌为例)
动物脑类器官培养基试剂盒(abs90050),基质胶(低因子、无酚红)(abs9495),15ml离心管(abs7102),1.5ml EP管若干(abs7119),24孔细胞培养板(abs7035)、金属冰盒。
动物脑类器官培养基试剂盒(abs90050)
基质胶(低因子、无酚红)(abs9495)
| 组分名称 | 规格 |
| 动物脑类器官培养基 A | 100ml |
| 类器官原代培养缓冲液 B | 250ml |
| 原代组织消化液 C | 30ml |
| 类器官传代消化液 D | 30ml |
| 组织保存液 E | 100ml |
| 类器官冻存液 F | 20ml |
| 类器官传代培养缓冲液 G | 250ml |
二、操作流程
1、加胶-点板-加液(这里是整个原代操作的点睛之笔)
(1)准备工作
a 基质胶需用金属冰盒盛放在4℃冰箱过夜融化
b 枪头、离心管需要-20℃提前预冷至少半小时
c 融化后的基质胶可一直放4℃储存,建议2周内用完

低温金属冰盒(abs7289)
(2)接种要求
24孔板(abs7035),每孔25ul基质胶细胞团混合物,500-750uL类器官培养液
(3)接种密度
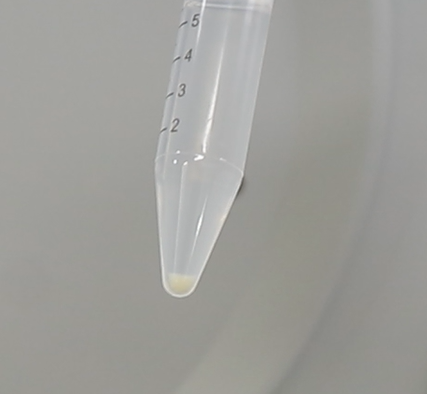 干细胞团沉淀
干细胞团沉淀
消化收集神经干细胞团到15ml离心管,于300g 4℃ 富集离心5min后移去上清。
密度建议1:基质胶体积:细胞团沉淀体积=25:1(如果估摸细胞团沉淀体积困难,通常加300uL基质胶足够)
密度建议2:500个细胞团/25uL基质胶(如果想计数接种,可以参照此密度建议)
(4)加胶-点板
向细胞团沉淀加入基质胶(abs9495),进行吹打混匀(不要满吹满打,容易产生气泡),然后进行点板。整个操作在金属冰盒或冰上进行。操作熟练以后,加胶,混匀,点板控制在半分钟内,有利于保持基质胶良好的流畅性。
(5)加液
将铺好的培养板放入37℃培养箱中40-60min成胶,添加500-750μl类器官培养基 A进行培养。大概10-14天,多数类器官直径在200um-500um,可进行传代操作。
 铺板密度
铺板密度
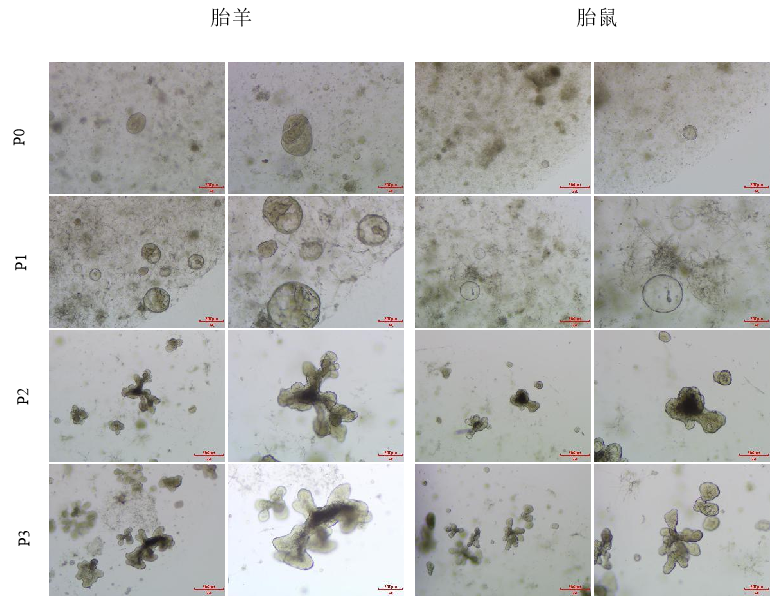 胎羊及胎鼠类器官生长图
胎羊及胎鼠类器官生长图
传代(消化分两种情况)
一、类器官数量较多或体积较大传代步骤
1、类器官收集及洗涤
1)收集:移液器吸去培养基,每孔添加 1-2ml 左右4℃类器官传代培养缓冲液G,轻柔吹散基质胶,收集在 15ml 离心管中(24孔板,每5孔为一组)。
2)洗涤:加类器官传代培养缓冲液G定容至14ml(缓冲液越多,基质胶被稀释的越充分,越容易去除),4℃静置 40min或-20℃放置5分钟(目的是使基质胶软化,如果冰箱保温效果强,缩短冷冻时间,摸索合适的冷冻时间时,可取出离心管摇晃看不到基质胶说明冷化好了)。
3)接下来将离心管进行300g,4℃, 离心5min,离心完通常会有这两种情况:
第一种是正常情况,分成三层(如下图),此时弃掉上清和基质胶层,保留类器官沉淀即可。
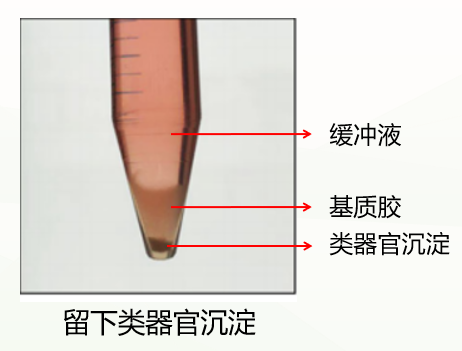
第二种是不正常情况,分成两层(如下图),这种情况可能与冷化不充分有关。此时弃掉缓冲液,留下基质胶类器官混悬液,重复上一步洗涤步骤,再次冷化离心,通常能出现清晰分层(缓冲液层、基质胶层、类器官沉淀层),此时弃掉上清和基质胶层,保留类器官沉淀即可。如果依然是两层(缓冲液层和基质胶类器官混悬液层),此时弃掉缓冲液和上1/3的基质胶类器官混悬液,保留下2/3即可。
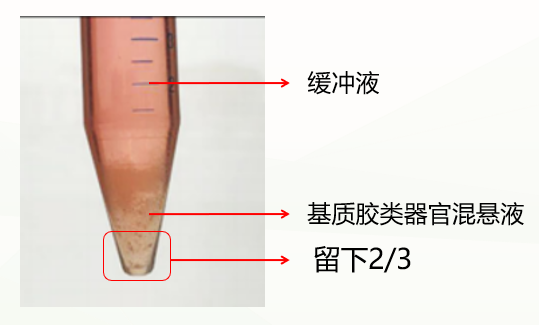
促进基质胶和类器官有效分离条件:
a离心机的选择非常重要,水平角离心机相比固定角离心机更利于基质胶和类器官分离;
b离心机的温度最好是4℃(可避免基质胶固化),离心转速可适当提高(最高不要超过500g),离心时间可适当加长(最常不超过10分钟)。
2、类器官消化
1)添加2-3mL类器官传代消化液D于超净台内消化2-3min,消化期间吹打1-2次。此步骤以消化成细胞团为主,千万不要消化成单细胞,单细胞类器官存活率低。如果不确定是否消化适宜,可吸取数微升镜下观察,如果有较多细胞团可停止消化。
2)添加5倍类器官传代培养缓冲液G(缓冲液:消化液=5:1)终止消化,300g 4℃ 离心 5min 弃去上清(如果有基质胶残留,残留量<50ul正常,不影响传代类器官增殖)

3、加胶-点板-加液
(1)准备工作
a 基质胶需用金属冰盒盛放在4℃冰箱过夜融化
b 枪头、离心管需要-20℃提前预冷至少半小时
c 融化后的基质胶可一直放4℃储存,建议2周内用完
(2)接种要求
24孔板(abs7035),每孔25ul基质胶细胞团混合物,500-750uL类器官培养液
(3)接种密度
密度建议1: 类器官通常按1:2传代,例如,24孔板收集5孔,传代10孔,需要的基质胶量25*10=250ul
密度建议2:500个细胞团/25uL基质胶(如果想计数接种,可以参照此密度建议)
注意:不管是按密度建议1还是,密度建议2,如果有残留的基质胶,新胶量至少是残留胶量的1.5倍
(4)加胶-点板
向细胞团沉淀加入基质胶(abs9495),进行吹打混匀(不要满吹满打,容易产生气泡),然后进行点板。整个操作在金属冰盒或冰上进行。操作熟练以后,加胶,混匀,点板控制在半分钟内,有利于保持基质胶良好的流畅性。
(5)加液
将铺好的培养板放入37℃培养箱中40-60min成胶,添加500-750μl人肠癌类器官培养基 A进行培养。大概10-14天,多数类器官直径在200-300um,可进行传代操作。
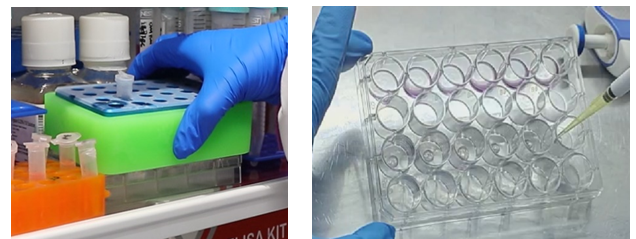
二、类器官数量不足或体积较小时:
1、类器官收集、吹打、洗涤
1)移液器吸去培养基,每孔添加 1-2ml 左右4℃类器官传代培养缓冲液G,轻柔吹散基质胶。
2)进行吹打,将类器官吹成细胞团(可取样镜下观察有较多细胞团时可停止吹打);
3)洗涤: 24孔板,每5孔为一组,收集在 15ml 离心管中,加类器官传代培养缓冲液G定容至14ml(缓冲液越多,基质胶被稀释的越充分,越容易去除),4℃静置 40min或-20℃放置5分钟(目的是使基质胶软化,如果冰箱保温效果强,缩短冷冻时间,摸索合适的冷冻时间时,可取出离心管摇晃看不到基质胶说明冷化好了)。
4)接下来将离心管进行300g,4℃, 离心5min,离心完通常会有这两种情况:
第一种是正常情况,分成三层(如下图),此时弃掉上清和基质胶层,保留细胞团沉淀即可。
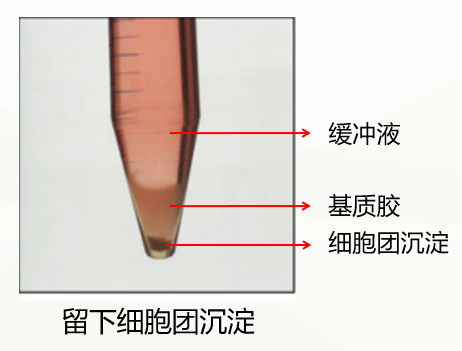
第二种是不正常情况,分成两层(如下图),这种情况可能与冷化不充分有关。此时弃掉缓冲液,留下基质胶类器官混悬液,重复上一步洗涤步骤,再次冷化离心,通常能出现清晰分层(缓冲液层、基质胶层、类器官沉淀层),此时弃掉上清和基质胶层,保留类器官沉淀即可。如果依然是两层(缓冲液层和基质胶细胞团混悬液层),此时弃掉缓冲液和上1/3的基质胶细胞团混悬液,保留下2/3即可。
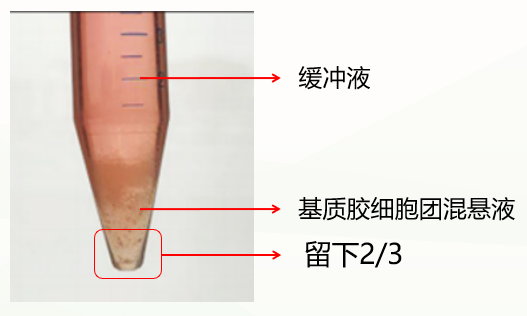
促进基质胶和类器官有效分离条件:
a离心机的选择非常重要,水平角离心机相比固定角离心机更利于基质胶和类器官分离;
b离心机的温度最好是4℃(可避免基质胶固化),离心转速可适当提高(最高不要超过500g),离心时间可适当加长(最常不超过10分钟)。
2、加胶-点板-加液
(1)准备工作
a 基质胶需用金属冰盒盛放在4℃冰箱过夜融化
b 枪头、离心管需要-20℃提前预冷至少半小时
c 融化后的基质胶可一直放4℃储存,建议2周内用完
(2)接种要求
24孔板(abs7035),每孔25ul基质胶细胞团混合物,500-750uL类器官培养液
(3)接种密度
密度建议1: 对于类器官数量较少的情况,为了维持生长所需的旁分泌信号,需要2-3孔富集到1孔,例如,24孔板收集6孔,2孔富集1孔,铺3孔,需要的基质胶量25*3=75uL
密度建议2:500个细胞团/25uL基质胶(如果想计数接种,可以参照此密度建议)
注意:不管是按密度建议1还是按密度建议2,如果有残留的基质胶,新胶量至少是残留胶量的1.5倍
(4)加胶-点板
向细胞团沉淀加入基质胶(abs9495),进行吹打混匀(不要满吹满打,容易产生气泡),然后进行点板。整个操作在金属冰盒或冰上进行。操作熟练以后,加胶,混匀,点板控制在半分钟内,有利于保持基质胶良好的流畅性。
(5)加液
将铺好的培养板放入37℃培养箱中40-60min成胶,添加500-750μl类器官培养基 A进行培养。大概7-10天,多数类器官直径在200-300um,可进行再次传代。
冻存
冻存要领:
类器官不需要消化(消化后的类器官复苏活率低);
在类器官指数增长期冻存(等到该传代的时候类器官活性比指数期差),也就传代后的Day3-Day4,多数类器官直径在100um-200um,这个时机选择冻存。
一、类器官收集及洗涤
1、收集:移液器吸去培养基,每孔添加 1-2ml 左右4℃类器官传代培养缓冲液G,轻柔吹散基质胶,收集在 15ml 离心管中(24孔板,每5孔为一组)。
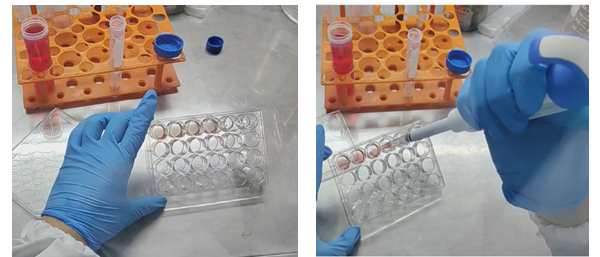
2、洗涤:加类器官传代培养缓冲液G定容至14ml(缓冲液越多,基质胶被稀释的越充分,越容易去除),4℃静置 40min或-20℃放置5分钟(目的是使基质胶软化,如果冰箱保温效果强,缩短冷冻时间,摸索合适的冷冻时间时,可取出离心管摇晃看不到基质胶说明冷化好了)。
3、接下来将离心管进行300g,4℃, 离心5min,离心完通常会有这两种情况:
第一种是正常情况,分成三层(如下图),此时弃掉上清和基质胶层,保留类器官沉淀即可。
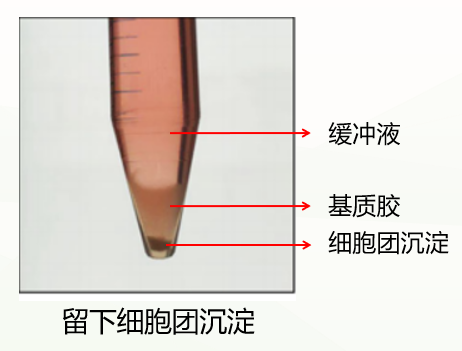
第二种是不正常情况,分成两层(如下图),这种情况可能与冷化不充分有关。此时弃掉缓冲液,留下基质胶类器官混悬液,重复上一步洗涤步骤,再次冷化离心,通常能出现清晰分层(缓冲液层、基质胶层、类器官沉淀层),此时弃掉上清和基质胶层,保留类器官沉淀即可。如果依然是两层(缓冲液层和基质胶类器官混悬液层),此时弃掉缓冲液和上1/3的基质胶类器官混悬液,保留下2/3即可。
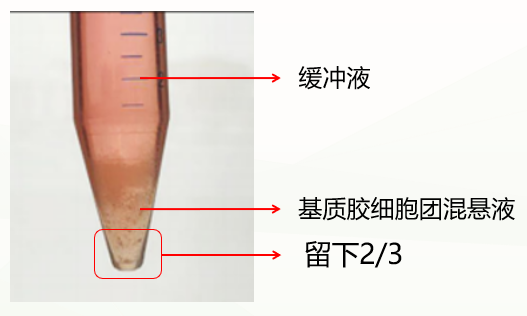
促进基质胶和类器官有效分离条件:
a离心机的选择非常重要,水平角离心机相比固定角离心机更利于基质胶和类器官分离;
b离心机的温度最好是4℃(可避免基质胶固化),离心转速可适当提高(最高不要超过500g),离心时间可适当加长(最常不超过10分钟)。
二、类器官冻存
1、冻存密度,以24孔板为例
密度建议1:2孔/mL 冻存液
密度建议2:500个类器官/mL 冻存液(如果想计数冻存,可以参照此密度建议)
2、添加适量类器官冻存液 F,轻柔吹打重悬,建议立即进行冻存。(放置太久,DMSO对类器官有损伤)
3、梯度冻存:将冻存管放入梯度冻存盒然后保存至-80℃过夜,第二天取出放入液氮罐。
手动冻存:4℃冰箱放置30 min,转移至-20℃放置1 小时,然后移至-80℃过夜,第二天取出放入液氮罐。
复苏
一、实验前准备
1、将水浴锅预热至37℃;
2、细胞实验室进行常规消毒,用预防喷雾喷涂并且使用紫外线照射40min的超净工作台台面;
3、在超净工作台中按次序摆好消过毒的离心管、吸管、培养板等。
二、取出冻存管
1、根据类器官冻存记录按标签找到所需类器官的编号。
2、从液氮罐中取出冻存盒,取出所需的冻存管,同时核对冻存管外的编号。
三、迅速解冻
1、迅速将冻存管投入到已经预热的水浴锅中解冻,并要不断地摇动,使管中地液体迅速融化。
2、约1-2min后冻存管内液体完全溶解,取出用酒精棉球擦拭冻存管地外壁,再拿入超净台内。
四、将类器官冻存液移入15ml离心管,添加10倍体积类器官传代培养缓冲液 G(缓冲液体积:冻存液体积=10:1)重悬,轻柔吹打混匀,300g 4℃ 离心 5min,弃上清。
五、加胶-点板-加液
1、准备工作
(1)基质胶需用金属冰盒盛放在4℃冰箱过夜融化
(2)枪头、离心管需要-20℃提前预冷至少半小时
(3)融化后的基质胶可一直放4℃储存,建议2周内用完
2、复苏要求
24孔板(abs7035),每孔25ul基质胶类器官混合物,500-750uL类器官培养液
3、复苏密度
复苏密度建议1:1:1接种(原来冻几孔就复苏几孔)
复苏密度建议2:250个类器官/25uL基质胶(如果想计数接种,可以参照此密度建议)
4、加胶-点板
向类器官沉淀加入基质胶(abs9495),进行吹打混匀(不要满吹满打,容易产生气泡),然后进行点板。整个操作在金属冰盒或冰上进行。操作熟练以后,加胶,混匀,点板控制在半分钟内,有利于保持基质胶良好的流畅性。
5、加液
将铺好的培养板放入37℃培养箱中40-60min成胶,添加500-750μl类器官培养基 A进行培养。大概10-14天,多数类器官直径在200um-500um,可进行传代操作。
6、脑类器官鉴定图
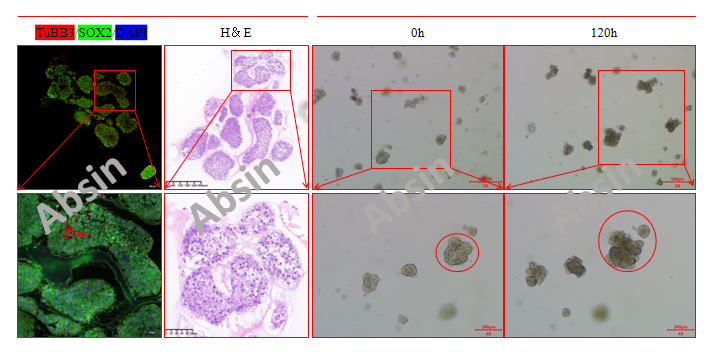
本期小爱推荐
| 货号 | 品名 | 规格 |
| abs9403 | 人多能干细胞培养基 | 500ml |
| abs9822 | 人多功能干细胞(PSC) 诱导神经干培养基 | 1kit |
| abs9821 | 神经干细胞(NSC)扩增培养基 | 1kit |
| abs9409 | 人多能干细胞消化液 | 100mL |
| abs9295-100mL | L-丙氨酰-L-谷氨酰胺溶液(100×,200mM) | 100mL |
| abs9412 | ES/iPS细胞冻存液 | 100mL |
| abs9410 | 即用型基质胶 | 100mL |
| abs90050 | Organotial动物脑类器官培养基试剂盒 | 1kit |
| abs9495 | 基质胶(低因子、无酚红) | 1.5ml*8 |
| abs7289 | 2mL低温金属冰盒(24孔,平底) | 1个 |
| abs7033 | 细胞培养板(标准透明6孔板) | 50个/箱 |
| abs7035 | 细胞培养板(标准透明24孔板) | 1箱 |
| abs7164 | 细胞冻存管 | 1箱 |
| abs7053 | 10mL一次性移液管 | 1箱 |
| abs7054 | 25mL一次性移液管 | 1箱 |










 危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)
危险品化学品经营许可证(不带存储) 许可证编号:沪(杨)应急管危经许[2022]202944(QY)  营业执照(三证合一)
营业执照(三证合一)