作为想发高分文章的研究者,一定会遇到如下情况:近期要安排一波8个样本的40种蛋白因子的分析检测,那您的安排是?

△点击放大图片
用WB来检测?
一张膜检测1个指标的话,需要做40张膜,如果再遇到几张显影效果不太好需要重来一遍的话,不知道2周是否可以完成整个实验呢?不眠不休的你实验结束后不知道黑眼圈会不会跟显影一个色号呢?

△点击放大图片
用ELISA来检测?
一块板子只能检测1个指标,那也需要做40块板子,如果实验室没有自动洗板机,那估计也得2周左右完成实验吧?而且不停的加试剂洗板,握移液枪的小手是不是都要麻木了呢?还有这么多数据需要统计整合,想想就很是酸爽...
如果再遇到 样本体积太少,不够做40个因子,只能放弃一些因子的检测么?
别急~~小优今天就来介绍一下大神们都在用的解放双手、节省时间、节省样本、节省经费的高效多因子技术,即同时检测多个样本的多个指标, 只需几个小时即可解决上述问题,并且在准确度、精确度、灵敏度方面与ELISA均可达到相似的水平!
那我们先来了解下目前都有 哪些多因子技术?
| 基因水平 | PCR Array |
| 蛋白水平 | MSD、luminex、CBA、Antibody Array |
| 组织水平 | 多重免疫组化(mIHC) |
这些多因子技术已经被应用到方方面面的领域,上述遇到的实验问题可以通过蛋白水平的多因子技术来解决,那上述的几种蛋白多因子技术有何区别,又该如何选择,小优整理了如下对比表格,可根据实验需求选择对应的检测方法。
| 蛋白多因子检测各技术对比表 | ||||
| - | MSD | Luminex | CBA | AntibodyArray |
| 样本类型 | 细胞/组织裂解液,血清,血浆,上清,脑脊液等 | 细胞/组织裂解液,血清,血浆,上清,脑脊液等 | 细胞/组织裂解液,血清,血浆,上清,脑脊液等 | 细胞/组织裂解液,血清,血浆,上清等 |
| 定量方式 | 超敏电化学发光 | 荧光定量 | 荧光定量 | 化学发光相对定量/荧光定量 |
| 灵敏度 | fg/mL级 | pg/mL级 | pg/mL级 | pg/mL级 |
| 可检测的因子数 | ≤10种(单孔) | ≤100种 | ≤30种 | ≤2000种 |
| 单孔样本需求量 | 低至25μL | 25-50μL | 50μL | 约300μg总蛋白 |
| 技术特点 | 高灵敏度、宽线性范围 | 高自由组合度,多指标(一块板同时检测几十种因子) | 不受孔板限制,自由度高 | 高通量初筛利器,多重WB,涵盖多种信号通路 |
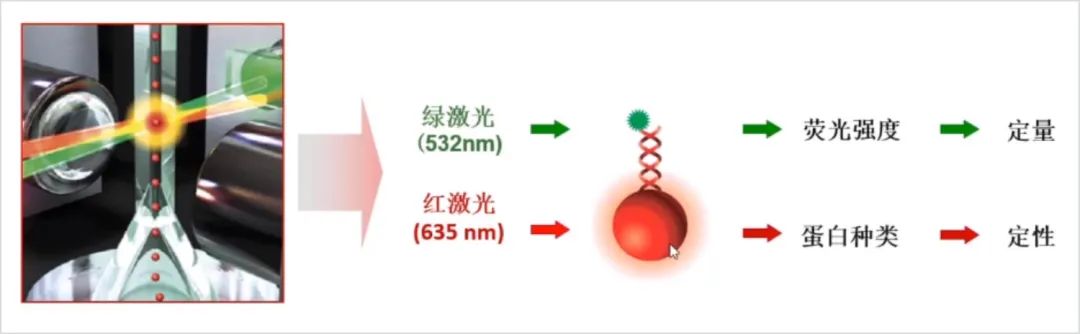
对比完各项蛋白多因子检测技术,今天我们重点聊聊可同时定量检测因子数最多的Luminex技术原理及其应用,来深入了解下这个一直被科研者青睐的宠儿~
△点击放大图片
Luminex xMAP技术又称为“液相悬浮芯片技术”,它有机整和了荧光编码微球技术、激光分析技术、流式细胞技术、高速数字信号处理技术、计算机运算法则等多项最新科技成果,将能识别不同目标分析物的微珠混合后与待检样本孵育,微珠捕获到分析物后,经由多个生物素标记的特异性检测抗体混合物识别,再与链霉亲和素-PE荧光素结合后进行检测,PE荧光的强度用以定量。可以实现高达100多种分泌性蛋白(细胞因子、趋化因子、生长因子等)的同时定量检测。
因其检测因子种类上的灵活性及因子数量上的优越性,Luminex xMAP技术已经被应用到各个领域用来研究信号通路、重大疾病、Biomarker开发、临床应用等,如免疫、炎症、肿瘤、心血管疾病、代谢、神经退行性疾病、细胞治疗等,分析物类型也多种多样,包含细胞因子、炎症因子、趋化因子、黏附因子脂肪因子、血管生成蛋白、肿瘤标记物、基质金属蛋白酶等。
Luminex技术应用如此广泛, 那我们下面就分别从 癌症、传染病及糖尿病研究方面, 具体来学习下 几篇高分文献中是如何应用该技术达到实验目的或者有了新发现的, 也重点给大家列出了 样本制备的方法哦, 干货较多,可能要多花费您几分钟的时间, 那我们就一起往下看吧。

△点击放大图片
Diagnostic and prognostic potential of the proteomic profiling of serum-derived extracellular vesicles in prostate cancer.
MicheleSignore.etal.CellDeathDis.2021
细胞外囊泡内含物质作为肿瘤的生物标志物,尤其作为液体活检领域的技术手段,具有巨大潜力。该研究利用基于抗体的蛋白质组学技术,即反相蛋白质微阵列(RPPA),来测量从前列腺癌患者血清中分离的细胞外囊泡中的关键抗原和激活的信号,发现了与临床环境相关的肿瘤特异性蛋白质谱以及基于细胞外囊泡的肿瘤诊断的候选标志物。
其中,PD-L1、ERG、Integrin-β5、Survivin、TGF-β、磷酸化的TSC2以及MAP激酶和mTOR通路等出现作为肿瘤来源的细胞外囊泡差异表达的终点。结果证实,血清衍生的细胞外囊泡可用于改进当前的诊断程序,同时提供潜在的预后和预测信息。这里提出的方法已经应用于除前列腺癌以外的肿瘤实体,从而证明了其在转化医学中的价值,并为开发具有临床意义的创新工具铺平了道路。

△点击放大图片
RPPA 技术是一种用于分析 EV 的强大生物标志物发现平台,首先选择合适的细胞系模型和通过差速超速离心条件培养基分离纯化EVs。扫描透射电子显微镜分析(SEM和 TEM)表明 90%富集到的EVs 范围从34到100nm。RPPA 和WB结果表明EVs跟外泌体一样会表达跨膜和胞质蛋白。
分别使用EpCAM表达为阳性和阴性的H1975和H1299肺癌细胞系(可用免疫电子显微镜证实),RPPA 测量了 A431和成纤维细胞中 EGFR_pY1068 的绝对量,虽然细胞来源的提取物展示出显着更高的数量,但随着A431来源的EV 混合比例增加,EGFR_pY1068的RPPA 表达在皮克范围以下仍可检测到,并用自制的 ELISA实验进行了验证。

△点击放大图片

△点击放大图片
对仅由 PCa 患者和健康个体 (HD) 组成的患者进行了 RPPA 实验,发现使用低至 37 种蛋白质分析血清来源的EV,根据它们在肿瘤过程中的相关性,就足以推断样本来源。而且ERG(ETS 相关基因)、PD-L1、Survivin、Integrin-β5、IL-6 和 SPARC 在肿瘤 EV 中显着改变。RPPA 分析关键 EV(磷酸)蛋白,例如那些参与 EGFR、mTOR和血管内皮生长因子受体(VEGFR)通路的机制靶点的蛋白,可针对癌症和患者采用治疗策略。
已知IL-6可促进前列腺肿瘤发生和进展为侵袭性,而可溶性血清蛋白成分如IL-6最终可能会在差异超速离心步骤后污染EV货物。
因此,作者设计了一个特别的实验,并通过Luminex技术对从血清来源的肿瘤EV的相同制剂中获得的两个配对样本进行了细胞因子分析。结果表明,虽然可溶性血清蛋白可能仍然是通过差速离心法制备的EV中不需要的污染物,但在这里,RPPA测量的IL-6水平可能主要来自EV货物。

△点击放大图片

△点击放大图片
为了确认上述初步实验结果,作者分析了一个更大的患者组。在所有比较组中达到统计显着性的关键终点,发现了MAP-激酶/mTOR通路的成分和相互作用物,如TGF-β、磷酸-β-Catenin_T41/S45(β-Catenin_pT41/PS45)
和磷酸-c-Myc_T58/S62。
该组分析的一部分蛋白质重现了上述实验中获得的差异表达模式。然后试图将关键的蛋白质组EV标志物与标准临床参数(例如前列腺特异性抗原(PSA)水平和pTNM)相关联。最终发现对于一些分析的标记,一小部分PCa样本与RPPA 表达水平方面的肥大性疾病。此外,有限数量的RPPA终点显示出与pTNM以及pTNM和PSA的相关趋势。
总体而言,RPPA对EV蛋白含量的分析揭示了一组癌症特异性生物标志物,并证明有针对性的液体活检方法可以区分患者和健康个体。我们的数据表明,将EV的蛋白质组学分析与常规临床参数相结合可能对早期癌症检测有用。

△点击放大图片
多因子检测样本制备
5ml外周血以1200rpm的速度离心5分钟收集血清,将血清转移到干净的管中并在PBS中稀释至等体积1.4ml。以1200rpm离心5分钟,将上清液转移到新管并再次以13300rpm离心15分钟。将上清液转移到干净的试管中并进行超速离心160000g(RCF),2小时。所有离心步骤均在4度下进行。洗沉淀后重悬于40μl磷酸盐缓冲盐水(PBS)中并测细胞外囊泡浓度。
100μg细胞外囊泡在50μl标准RIPA缓冲液中裂解(加蛋白酶抑制剂,用蒸馏水补至体积);并用PBS按1:4稀释用于分析。再用同样的100μg未裂解的细胞外囊泡,最后一步超速离心后加入50μl PBS缓冲液中直接用于luminex分析。细胞外囊泡提取物和未裂解的细胞外囊泡中的细胞因子/趋化因子用通过Luminex平台的xMAP技术进行定量检测。PBS稀释了4倍的RIPA缓冲液和PBS缓冲液用作背景对照。
检测指标
BDNF、CCL11、FGF-13、IL-5、IL-4、IL-23、IL-6、MMP-2、beta-NGF、N-regulin-1beta1/NRG-1、TNF-α、CXCL10、IFN-γ、IL-2、IL-8/CXCL8、IL-17/IL-17A、CCL-2/MCP-1和VEGF
所用试剂盒

△点击放大图片
下面我们再简单学习下Luminex多因子技术在传染病和糖尿病中是如何被运用并得到一些洞见的。

△点击放大图片
Altered differentiation is central to HIV-specific CD4+ T cell dysfunction in progressive disease.
AntigoniMorou.etal.NatImmunol.2019
病毒特异性CD4+T细胞在人类慢性感染病中的功能障碍研究不是很多,本研究针对感染了人类免疫缺陷病毒(HIV)并用了抗逆转录病毒疗法(ART)的患者,对其治疗前和后的特异性CD4+T细胞进行全基因组转录分析和功能分析。
为控制病毒自发产生的HIV特异性的CD4+T会强烈表达与TH1、TH17相关的基因和辅助T细胞的TH22亚群。与自发产生的病毒特异性细胞相比,经ART后病毒受到抑制会导致了不同的转录分化,与TFH细胞相关的基因表达减少,并伴有TH1、TH17和TH22细胞相关的基因低表达。
因此,分化的改变是HIV特异性CD4+T功能障碍的关键因素,这包括功能的获得和功能的丧失。
多因子检测样本制备
PBMC是Ficoll密度梯度法分离,然后用磁珠阴性分选法去除cd8 T细胞。用HIV Gagpe ptidepool (1μg/ml/peptide) 感染100万个去除CD8的PBMC细胞,与未刺激的细胞一起放在添加了10% HAB和抗生素的RPMI中37度培养。刺激48小时后收集细胞培养上清,用高敏细胞因子检测试剂盒在Luminex平台上进行检测,CXCL13指标单独用Elisa试剂盒检测。
检测指标
IL-2,IFN-γ,TNF-α,IL-17A,IL-22,IL-31和IL-17F;CXCL13
所用试剂盒

△点击放大图片

△点击放大图片
Targeted Elimination of Senescent Beta Cells Prevents Type 1 Diabetes. PeterJ.Thompson.etal.CellMetab.2019
1型糖尿病(T1D)是一种器官特异性自身免疫性疾病,其特征是由于高血糖胰腺β细胞逐渐丧失而导致的高血糖症。免疫介导的β细胞破坏导致了这种疾病,但β细胞是否积极参与发病机制尚不清楚。
本文展示了在人类1型糖尿病和非肥胖糖尿病(NOD)小鼠模型的自然病程中,一部分β细胞获得了衰老相关的分泌表型(SASP)。衰老的β细胞上调了促生存介质Bcl-2, 用Bcl-2抑制剂治疗NOD小鼠选择性地消除了这些细胞,而不会改变与疾病相关的免疫细胞类型的丰度。值得注意的是, 消除衰老的β细胞可以阻止免疫介导的β细胞破坏, 可作为一种新的T1D治疗方法。
多因子检测样本制备
将从胰腺中分离得到的胰岛在含有 5.5 mM 葡萄糖、10% FBS和1X青霉素-链霉素或1X抗生素-抗真菌剂的RPMI-1640中培养。根据实验方案对胰岛进行不同条件处理后,将胰岛转移到无血清人胰岛培养基中培养24小时,以500 g离心5分钟将胰岛与培养基分离,收集上清液用于luminex实验。
检测指标
小鼠胰岛细胞IL-6, Mmp9, Mmp12, Igfbp3, Ccl2, G-Csf, Serpine1, IL-2, Granzyme B, Glucagon和 Pancreatic Polypeptide。
人胰岛细胞 IL-6, IL-8, CXCL10,CXCL1, MMP3, G-CSF, IGFBP4, MMP9
所用试剂盒

△点击放大图片
另外还有关于Luminex多因子技术在细胞治疗和过敏性疾病中的应用,详情可查看以下文献:
A safe and potent anti-CD19 CAR T cell therapy.
ZhitaoYing.etal.NatMed.2019
Innate and adaptive immune responses in asthma.
StephenTHolgate.NatMed.2012
多因子检测作为高效的检测手段,被广泛应用在多种疾病研究中, LabEx可以提供包括MSD、Luminex、CBA以及抗体芯片在内的多因子检测服务。详情可联系我们。
部分多因子检测服务爆款试剂盒:
| 检测技术 | 试剂货号 | 因子数 | 检测因子 |
| Luminex | LX-MultiDTX-44 | 44 | CCL2/JE/MCP-1,CCL3/MIP-1alpha,CCL4/MIP-1beta,CCL5/RANTES,CCL11/Eotaxin,CCL19/MIP-3beta,CCL20/MIP-3alpha,CD40Ligand/TNFSF5,CXCL1/GROalpha/KC/CINC-1,CXCL2/GRObeta/MIP-2/CINC-3,CXCL10/IP-10/CRG-2,EGF,FGFbasic/FGF2/bFGF,Flt-3Ligand/FLT3L,G-CSF,GM-CSF,GranzymeB,IFN-alpha2/IFNA2,IFN-beta,IFN-gamma,IL-1alpha/IL-1F1,IL-1beta/IL-1F2,IL-1ra/IL-1F3,IL-2,IL-3,IL-4,IL-5,IL-6,IL-7,IL-8/CXCL8,IL-10,IL-12p70,IL-13,IL-15,IL-17/IL-17A,IL-17E/IL-25,IL-33,PD-L1/B7-H1,PDGF-AA,PDGF-AB/BB,TGF-alpha,TNF-alpha,TRAIL/TNFSF10,VEGF |
| Luminex | LX-MultiDTX-48 | 48 | FGF-basic,Eotaxin,G-CSF,GM-CSF,IFN-γ,IL-1β,IL-1rα,IL-1α,IL-2Rα,IL-3,IL-12(p40),IL-16,IL-2,IL-4,IL-5,IL-6,IL-7,IL-8,IL-9,GRO-α,HGF,IFN-α2,LIF,MCP-3,IL-10,IL-12(p70),IL-13,IL-15,IL-17,IP-10,MCP-1(MCAF),MIG,β-NGF,SCF,SCGF-β,SDF-1α,MIP-1α,MIP-1β,PDGF-BB,RANTES,TNF-α,VEGF,CTACK,MIF,TRAIL,IL-18,M-CSF,TNF-β |
| Luminex | LX-MultiDTM-23 | 23 | IL-1α, IL-1β, IL-2, IL-3, IL-4, IL-5, IL-6,IL-9, IL-10, IL-12 (p40),IL-12 (p70), IL-13,IL-17A, Eotaxin, G- CSF, GM-CSF, IFN-γ, KC, MCP-1 (MCAF), MIP-1α, MIP-1β, RANTES,TNF-α |
| Luminex | LX-MultiDTH-27 | 27 | FGF basic, Eotaxin, G-CSF, GM-CSF, IFN-γ, IL-1β, IL-1rα, IL-2, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-12(p70), IL-13, IL-15, IL-17, IP-10, MCP-1(MCAF), MIP-1α, MIP-1β, PDGF-BB, RANTES,TNF-α, VEGF |
| Luminex | LX-MultiDTM-31 | 31 | BCA-1/CXCL13, CTACK/CCL27, ENA-78/CXCL5, Eotaxin/CCL11, Eotaxin-2/CCL24, Fractalkine/CX3CL1, GM-CSF, I-309/CCL1, IFN-γ, IL-1β, IL-2, IL-4, IL-6, IL-10, IL-16, IP-10/CXCL10, I- TAC/CXCL11, KC/CXCL1, MCP-1/CCL2, MCP-3/CCL7, MCP-5/CCL12, MDC/CCL22, MIP-1α/CCL3, MIP-1β/CCL4, MIP-3α/CCL20, MIP-3β/CCL19, RANTES/CCL5, SCYB16/CXCL16, SDF-1α/CXCL12, TARC/CCL17, TNF-α |
| MSD | LX-K15049D | 10 | IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-8,IL-10,IL-12p70,IL-13,TNF-α |
| MSD | LX-K15048D | 10 | IFN-γ,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-10,IL-12p70,KC/GRO,TNF-α |
| CBA | abs590001 | 10 | IFN-Gma、IL-1Bta、IL-2、IL-4、IL-6、IL-8、IL-10、IL-12P70、IL-17A、TNF |
| CBA | 560484 | 7 | IL-2,IL-4,IL-6,IL-10,TNF,IFN-g,IL-17A |
| AntibodyArray | ARY003C | 39 | Akt1/2/3(S473),HSP60,PRAS40(T246),Akt1/2/3(T308),JNK1/2/3(T183/Y185,T221/Y223),Pyk2(Y402),beta-Catenin,Lck(Y394),RSK1/2(S221/S227),Chk-2(T68),Lyn(Y397),RSK1/2/3(S380/S386/S377),c-Jun(S63),MSK1/2(S376/S360),Src(Y419),CREB(S133),p38alpha(T180/Y182),STAT1(Y701),EGFR(Y1086),p53(S15),STAT2(Y689),eNOS(S1177),p53(S392),STAT3(S727),ERK1/2(T202/Y204,T185/Y187),p53(S46),STAT3(Y705),Fgr(Y412),P70S6Kinase(T389),STAT5a/b(Y699),GSK-3alpha/beta(S21/S9),p70S6Kinase(T421/S424),STAT6(Y641),GSK-3beta(S9),PDGFRbeta(Y751),WNK-1(T60),HSP27(S78/S82),PLCgamma-1(Y783),Yes(Y426) |