肠道是人体重要的消化器官
肠指的是从胃幽门至肛门的消化管,是消化管中最长的一段,也是功能最重要的一段。
△点击放大图片
炎症性肠病,简称IBD,是一种特殊的慢性肠道炎症性疾病,主要包括克罗恩病(CD)和溃疡性结肠炎(UC)。近30年来,我国IBD发病率有不断攀升的趋势。根据国内文献报道,近5年的病例数是上世纪90年代同期的8倍,IBD已逐渐成为我国消化科的常见病。
肠道cDC的功能


△点击放大图片
(a) cDC在小肠LP中起作用。通过SLRPa+CD103+CD11b+cDC和SLRPa+CD103-CD11b+cDC感知鞭毛蛋白,可能诱导IL-23分泌,导致ILC3激活和IL-22分泌。由SIRPa+cDC产生的IL-23也被描述为限制XCR1+cDC对IL-12的分泌。XCR1+cDC是主要的APC,它吸收细胞来源的抗原进行交叉呈递给CD8+T细胞。此外,它们已被证明通过整合素avb8产生活性TGFb,促进CD8aa+CD4+细胞毒性的发育,并通过XCR1/XCL1轴维持肠道T细胞的存活。最后,肠道淋巴细胞产生的XCL1参与了诱导XCR1+cDC中CCR7的表达,并促进其向MLN的迁移。
(b)cDC在肠淋巴结中起作用。XCR1+cDC在诱导CD8+T细胞对交叉呈递抗原的应答方面具有优势,是产生RA的主要cDC亚群,诱导应答CD4+(橙色细胞)和CD8+(蓝色细胞)T细胞上CCR9的表达。它们也促进Th1的诱导,但抑制Th2反应的发展。
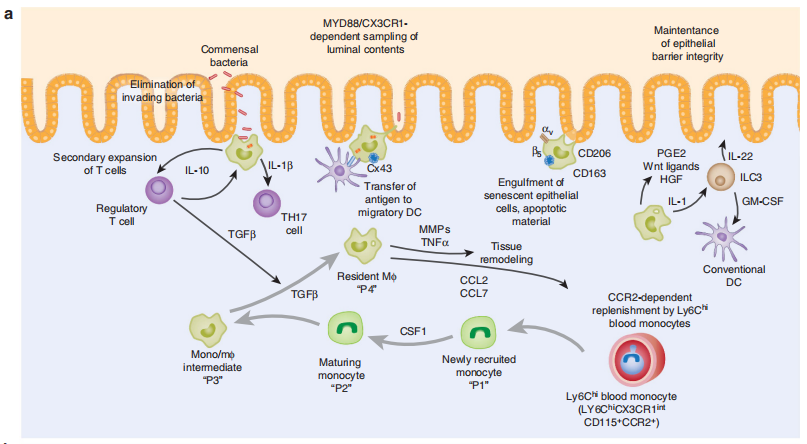
巨噬细胞与肠道中健康和炎症

△点击放大图片
(a) 在稳定状态的成人肠道中,Ly6Chi单核细胞以ccr2依赖的方式不断地从血液中出现。到达粘膜后,他们发展通过“单核细胞瀑布”,LyChi MHCII CX3CR1int F4/80lo单核细胞,获得MHCII,在失去Ly6C成为Ly6CMHCII+F4/80+单核/巨噬细胞中介,最后获得高水平的CX3CR1作为他们最终分化成大多数居民巨噬细胞。这一过程由特定于肠道微环境的因素决定,最后一步至少部分依赖于TGFb。常驻巨噬细胞参与重要的稳态功能,因为它们具有强烈的吞噬活性,并产生细胞因子和趋化因子。因此,巨噬细胞可以与局部免疫细胞如T细胞和ILC细胞相互作用。所有这些活动都在没有发生炎症的情况下发生,这是由于来自T细胞和巨噬细胞的IL-10阻止了激活,也因为抑制巨噬细胞中PRR信号的内在机制。由驻留的巨噬细胞产生的IL-10也能驱动已在淋巴结中启动的FoxP3+Treg的二次扩增和存活。
(b)粘膜炎症可由侵袭性病原体、上皮屏障损伤导致共生细菌暴露增加,或巨噬细胞控制途径如NOD2或IL-10功能缺陷引起。在这种情况下,Ly6Chi单核细胞的募集增强,正常的分化过程被破坏,允许促炎单核细胞和早期中介巨噬细胞的积累。这些介质释放炎症介质,如NO、ROI、TNFa、IL-12、IL-23、IL-6和IL-1b,引起组织损伤,并激活其他炎症细胞,包括Th1或Th17效应细胞。预先存在的常驻巨噬细胞可能导致这些炎症事件。单核细胞还可以通过释放pge2来帮助抑制病理,从而抑制中性粒细胞的有害影响。
炎症性肠病(IBD)中两类疾病中的细胞因子
△点击放大图片
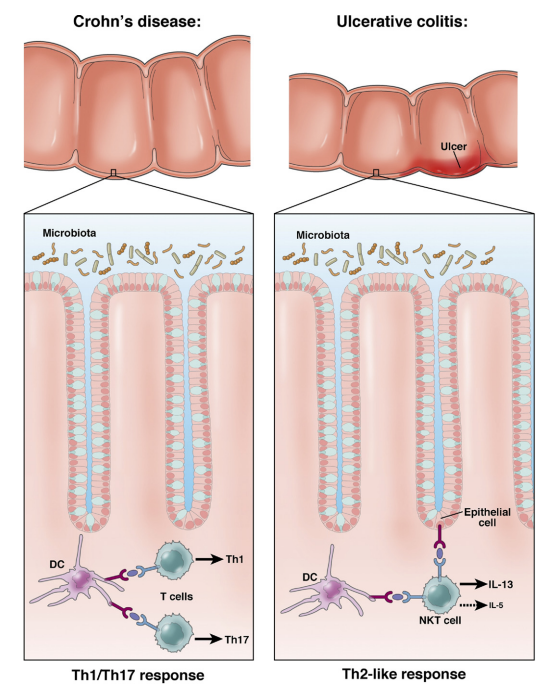
虽然克罗恩病和溃疡性结肠炎都是IBD的形式,并表现出重叠的基因谱,但这些疾病的特征是非常不同的t细胞反应。克罗恩病是由t辅助细胞(Th)1/Th17反应驱动的,其中IL-12和IL-23细胞因子发挥关键作用。相比之下,溃疡性结肠炎是由th2样反应驱动的,其中产生IL-13(和IL-5)的NKT细胞是主要反应。此外,在这两种形式的IBD中,同时具有这些基本细胞因子的“上游”和“下游”功能的细胞因子也发挥着重要的炎症作用。
t细胞分化途径和肠道炎症
在1980年代末发现,Th细胞分化为Th1和Th2细胞,并产生不同的细胞因子,CD中似乎是Th1细胞因子介导的疾病,并增加产生干扰素;而UC似乎是Th2细胞介子介导的疾病,特点是增加产生白细胞介素(IL)-5和IFN的产生。然而,需要注意的是,UC中Th2反应的特征细胞因子(IL-4)的产生没有增加,很明显,后者是一种“Th2样”疾病,而不是一种完全的Th2疾病。
由t辅助细胞Th17反应启动的调节机制
△点击放大图片
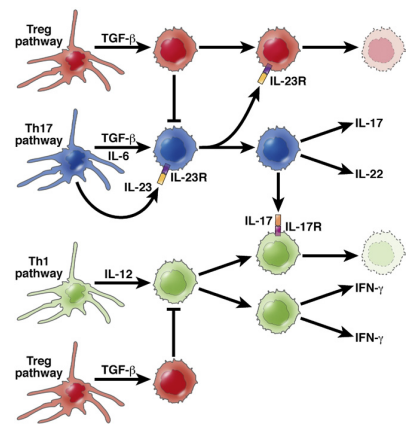
总之,现在似乎很清楚,尽管Th17反应有可能成为促炎反应时存在足够的数量,它更有可能功能主要作为监管反应在实验结肠炎模型,Th17细胞的数量可能是有限的。
在这张图中,Th17反应(用蓝色的细胞表示)产生产生IL-17和IL-22的细胞,后者是一种明显已知的改善肠道炎症的细胞因子。这种反应依赖于IL-23的产生,IL-23也抑制调节性T细胞(Treg)的生成(用红色的细胞表示),并抵消Treg对Th1(干扰素-[IFN-])和Th17(IL-17)促炎反应的抑制作用。相比之下,IL-17通过IL-17受体与IFN-产生细胞(如绿色细胞所示)的相互作用抑制了IFN-产生细胞的生成。因此,Th17反应同时允许和抑制Th1反应,可能是在炎症周期的不同阶段。
CD疾病中Th1和Th17细胞因子的反应

△点击放大图片
t辅助细胞(Th)1和Th17反应处于共存的稳定状态在这张图中,提出了克罗恩炎症由无数的微环境组成,每个微环境都表现出炎症模式的进展。在炎症的初始和最强烈的阶段,Th1反应占主导地位;此时,新生的Th17反应中IL-23的产生抑制了调节性t细胞(Treg)的生成并促进炎症。在后期阶段,混合T细胞反应盛行,其中Th1反应仍然占主导地位,但现在被Th17反应调节,产生白细胞介素(IL)-17和IL-22。
细胞因子反应在慢性TNBS-cromit是Th1和Th17反应是分开的,这表明人类肠道炎症通常以连续的反应改变Th1和Th17细胞病变成熟。这一概念与Th1和Th17分化的反调控特性相一致,即IL-17具有抑制IFN-产生T细胞的趋势,反之亦然。这与最近的异种共生和共转移研究相一致,表明Th1和Th17相互竞争并相互下调。
UC疾病中的细胞因子反应
△点击放大图片
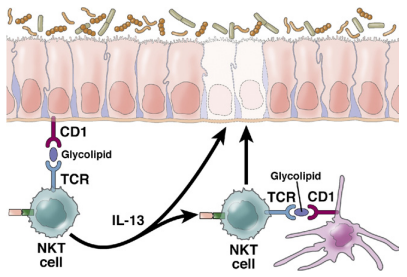
溃疡性结肠炎的炎症是由微生物群或上皮细胞所产生的糖脂抗原引起的。这些抗原在上皮细胞或树突状细胞表面的CD1背景下呈现给NKT细胞,因此受到刺激的NKT细胞作为效应细胞介导疾病。由此导致的上皮细胞损伤和溃疡形成是由NKT细胞的细胞毒性活性引起的,NKT细胞识别携带装载抗原的CD1的上皮细胞为靶点,或通过IL-13,已被证明会导致上皮细胞凋亡和上皮屏障功能的丧失;此外,IL-13增强了NKT细胞的细胞毒性。
在最后一系列的研究中,评估了NKT细胞和/或IL-13介导组织损伤的潜力。结果发现,纯化的固有层CD4T细胞对脂多糖(LPS)预刺激的HT-29上皮细胞具有上调CD1d,而IL-13增强了这种细胞毒性。此外,观察到IL-13通过诱导上皮细胞凋亡和增加孔形成紧密连接蛋白claudin-2.67的表达来降低HT-29上皮细胞单层的电阻。这些研究表明,UC疾病固有层中NKT细胞的存在可通过NKT细胞介导的细胞毒性导致溃疡和炎症;此外,IL-13促进组织损伤,它增强了NKT细胞的细胞毒性,并影响上皮细胞的完整性。
肠道炎症中的TL1A
△点击放大图片
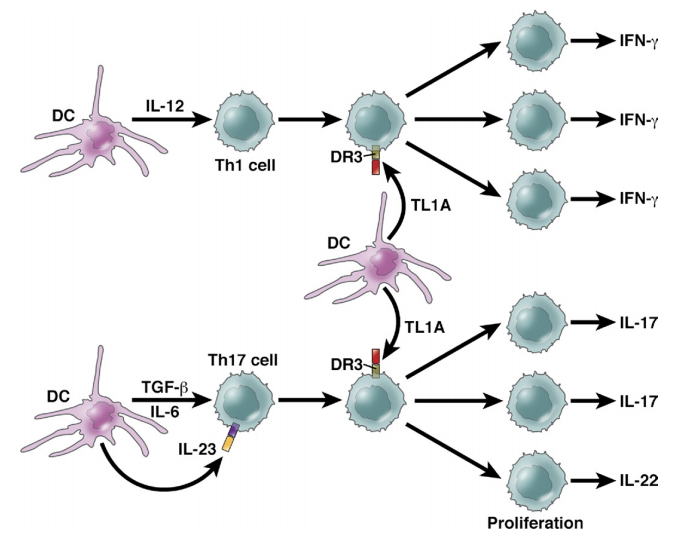
TL1A是一个肿瘤坏死因子家族成员,仅通过DR3发挥作用。它的促炎功能连接了t辅助细胞(Th)1/Th17Th2二分法,因为它增强了两种类型的t细胞反应。如图,Th1或Th17分化导致T细胞表达DR3(TL1A受体),然后受到TL1A共刺激,后者是最佳增殖和细胞因子反应所必需的。Th2细胞以类似的方式被共同刺激。TL1A还有其他作用,如调节性T细胞也可能导致炎症。
小知识
肠道中常见细胞亚群:
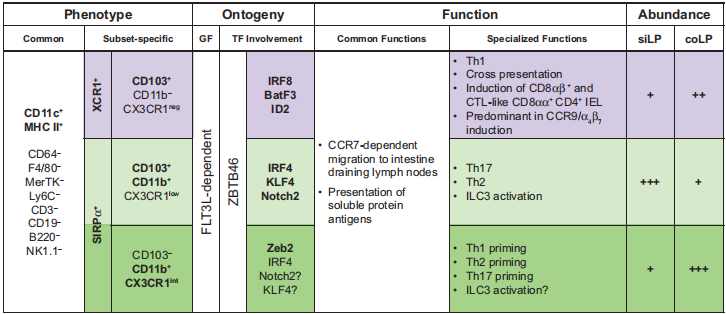
△点击放大图片
肠内的单核细胞和巨噬:
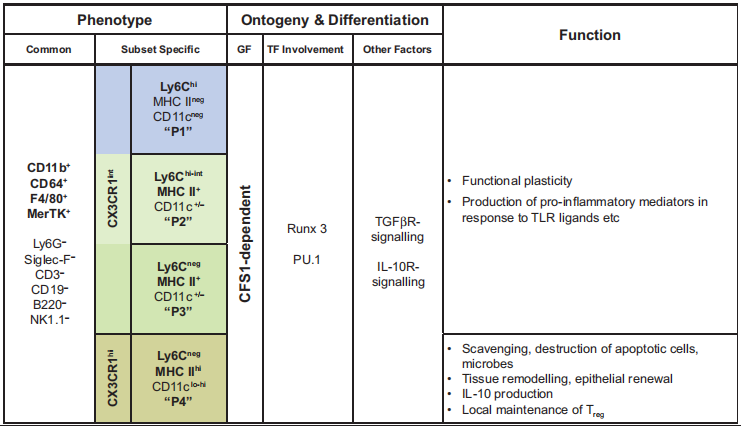
△点击放大图片
Reference:
[1].Diversity and functions of intestinal mononuclear phagocytes.
[2].Proinflammatory Cytokines in the Pathogenesis of Inflammatory Bowel Diseases.