2022年度国自然医学部科研热点中标数量统计排名中,免疫调控以中标书907项依旧是稳居第一!此外,值得我们关注的是巨噬细胞,较上年度中标数激增,以591项中标数名列第二名!当然第一名免疫调控也与巨噬细胞有着紧密的联系,可见巨噬细胞作为现在科研话题的热度之高,重要性之强!
此外关于肿瘤相关巨噬细胞(TAMs)的研究也是势不可挡!在pubmed中搜索关键词“tumour-associated macrophages”,仅2022年就有上千篇文章发表,其中有多篇为顶级期刊高分文章,可见肿瘤巨噬细胞的研究已经强势来袭!!!好了,话不多说,跟着小优一起来了解TAMs吧!
01巨噬细胞
巨噬细胞的发现
巨噬细胞(Macrophages)发现于1882年,生物学家Ellie Metchnikoff在研究缺乏适应性免疫机制的原始动物时发现了它们,当时将这类细胞称为吞噬细胞。巨噬细胞作为人体中非常重要的免疫细胞类型,通常被认为是由骨髓中的单核细胞发育而来。
巨噬细胞是什么?
巨噬细胞是一种广泛分布于机体血液、组织的免疫细胞。它能够吞噬和杀灭胞内寄生虫、细菌、肿瘤细胞、以及自身衰老和异常的细胞,在机体的免疫防御、免疫自稳和免疫监视中发挥重要作用。此外,可释放多种免疫因子激活其它适应性免疫细胞,为T细胞呈递外来抗原,参与激发适应性免疫功能。
巨噬细胞的功能
❖吞噬作用
巨噬细胞作为专职的吞噬细胞,要正常发挥其生理功能,其吞噬作用是功不可没的。在人体中,巨噬细胞大部分以游离的细胞形式存在于血液中,当人体出现疾病炎症时,血液中出现的大量坏死细胞残片、病原微生物体等正是巨噬细胞最好的食物。巨噬细胞外周有大量的纤毛,它们通过纤毛运动发挥其独特的噬菌作用,将坏死的细胞残片或病原微生物吞噬并消化掉,同时激活人体的淋巴系统,向机体内其它免疫细胞发出信号,并建立起一道人体的防线。
❖巨噬细胞的极化作用
巨噬细胞具有异质性和多样性,可在组织微环境和生理病理条件下,转化为不同的表型,即经典活化性巨噬细胞(classically activated macrophage,M1)和选择活化性巨噬细胞(alternatively activated macrophage,M2)。
经典激活——M1型巨噬细胞:可以由IFN-γ、LPS或GM-CSF诱导,通过释放IL-1等炎性介质,促进炎症反应,杀伤胞内感染的病原体,增强抗肿瘤免疫的能力。
交替激活——M2型巨噬细胞:由IL-4、IL-13等诱导,高表达CD206,内吞能力增强,分泌IL-10、TGF-β等抑炎性细胞因子,促进Th2细胞分化,发挥抗炎作用,参与免疫调节、修复功能、伤口愈合、血管生成、促进肿瘤生长和转移。
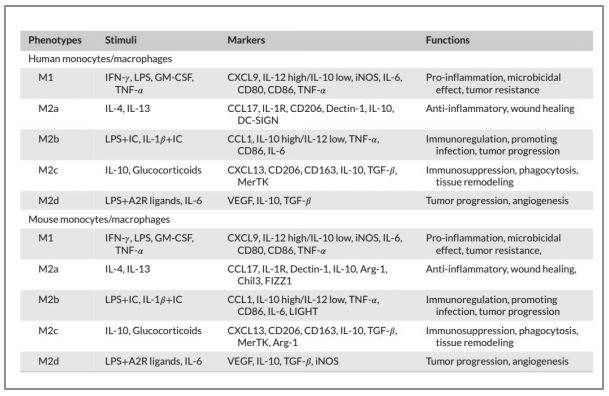
Figure 1 M2b macrophage polarization and its roles in diseases
不同极化状态巨噬细胞标志物和功能
△点击放大图片
❖抗原呈递
巨噬细胞作为抗原呈递细胞,是启动和调节免疫反应的前哨。巨噬细胞捕获、内吞和表达自身或外来抗原,提呈给其他免疫细胞,作为启动免疫反应的一部分;还可分泌不同的趋化因子和各种强大的物质,影响适应性免疫细胞的激活。
02巨噬细胞与肿瘤免疫治疗
慢性炎症已被证实是癌症病发前期的重要因素之一,它会导致持续表达免疫相关转录因子激活多种细胞因子和趋化因子,进而促进多种免疫细胞的招募,其中就包括巨噬细胞。当巨噬细胞被招募到炎症组织之后,会进一步释放更多的促炎症反应的因子。多种因素共同创造了“促进基因突变产生”的微环境——肿瘤微环境(tumormicroenvironment ,TME)。这种复杂且动态的生态系统,有很多不同细胞群共存,也为肿瘤的发生和发展提供了基本的生态位。在肿瘤组织中,肿瘤相关巨噬细胞(TAMs:Tumor-associated macrophages)是最主要成分;对于TAMs的研究,人们一开始认为它是抗肿瘤效应细胞,但随着研究的深入,人们发现TAMs的主要作用是促肿瘤、免疫抑制等,是肿瘤发展、转移和耐药性的关键诱导因素,因此也成为了肿瘤免疫治疗领域热门靶标。
03肿瘤相关巨噬细胞
肿瘤相关巨噬细胞如何生成
TAMs是组织癌变之后巨噬细胞的新身份。目前认为TAMs的主要来源包括两种,分别为骨髓来源的单核细胞浸润至肿瘤微环境形成TAMs和组织驻留巨噬细胞受肿瘤教化形成TAMs,二者的分化和扩散均受到CSF1R及其配体IL-34和CSF1的调控。
肿瘤相关巨噬细胞与M1/M2型巨噬细胞的关系
肿瘤细胞衍生的细胞因子(如IL-10和CSF1),以及趋化因子(如CCL2、CCL18、CCL17和CXCL4),是促肿瘤模式下TAMs功能可塑性的关键促进剂。由于肿瘤微环境以缺氧、弱酸性为主要特征,导致TAMs在肿瘤部位多呈现M2表型。M2-TAMs表现出多项促肿瘤作用:
(1)抑制肿瘤免疫反应,特别是T细胞介导的细胞毒性;
(2)诱导肿瘤血管生成;
(3)参与肿瘤迁移,侵袭和转移;
(4)增强肿瘤化学疗法和放射疗法的耐药性。
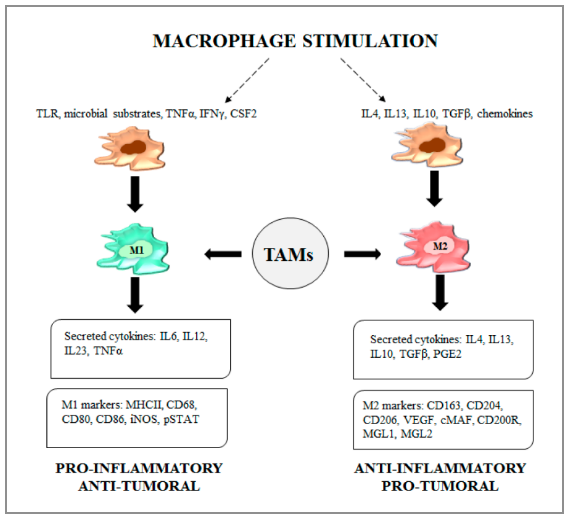
Figure 2 Tumor-Associated Macrophage Status inCancer Treatment M1和M2型肿瘤相关巨噬细胞
△点击放大图片
肿瘤相关巨噬细胞促进肿瘤和抑制免疫途径
❖通过分泌PDGF、EGF促进肿瘤细胞增值;
❖通过分泌IL1、CSF-1、MMPs(eg:MMP2、MMP9)等促进肿瘤细胞的转移和浸润;
❖通过产生IL10、PGE2、TGFβ等参与肿瘤细胞的免疫抑制和调控;
❖通过表达VEGF参与肿瘤微血管与淋巴管的生长;
❖通过调控肿瘤细胞代谢以促进肿瘤生长;
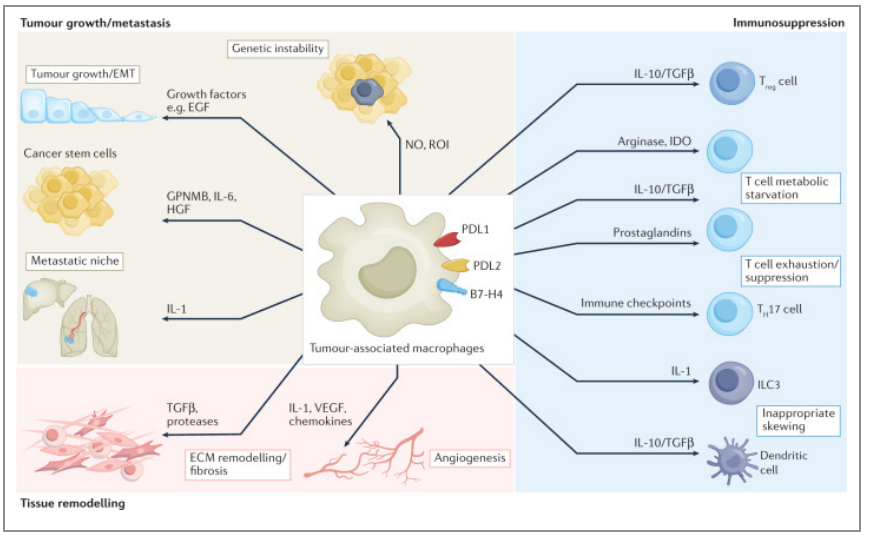
Figure 3 Macrophages as tools and targets in cancer therapy
△点击放大图片
TAMs促肿瘤功能及免疫抑制途径
04巨噬细胞免疫治疗的应用
肿瘤治疗中的TAMs调控策略
目前学者们已经针对TAMs的相关特性来进行药物开发,以TAMs为靶点的肿瘤治疗调控策略主要可分三种:
❖TAMs耗竭:抑制肿瘤相关巨噬细胞的产生和促进其衰竭;
❖抑制TAMs募集:抑制肿瘤相关巨噬细胞的招募;
❖TAMs复极化:重编程肿瘤相关巨噬细胞,使其从抑制肿瘤免疫状态变为促进肿瘤免疫状态;
相比于TAMs耗竭和抑制TAMs募集策略,TAMs复极化策略不仅使免疫抑制型TAMs减少,还使促炎表型巨噬细胞增加,可更高效地逆转免疫抑制型TME。同时,该策略避免了巨噬细胞急剧减少对正常组织的影响。因此,TAMs复极化策略在肿瘤免疫治疗领域也受到更广泛的关注。
目前靶向调控TAMs的策略已经成为一种多机制、多功能的高效疗法,并能改善化疗耐药和不良预后。与化疗等经典疗法相比,TAMs调控策略是通过调节自身免疫系统功能对抗肿瘤,对患者正常组织的损伤较小。因此,目前针对TAMs的新型调控策略在肿瘤免疫治疗以及与其他疗法的联合治疗中也均表现出巨大的潜力。
TAMs的热门靶点
目前以TAMs为靶点的单一疗法或联合化疗的治疗方法正在临床中进行试验。现在临床上进展较快的主要靶点有:CSF-1R、CD47、巨噬细胞微环境趋化因子等。
❖TAMs被CSF-1招募到TME中,促进乳腺癌的发展和转移。目前用单克隆抗体或小分子化合物靶向CSF-1/CSF-1R轴的治疗方法也正在试验中。
❖靶向CSF-1R、c-Kit和Flt3的酪氨酸激酶抑制剂PLX3397通过使TAMs的M2表型去极化来阻断肿瘤进展。
❖CD47是一种广泛分布于正常细胞表面的免疫球蛋白,可通过抑制吞噬作用负调节抗肿瘤免疫。给予CD47阻断抗体或靶向灭活CD47基因可显著抑制肿瘤生长。
CAR-巨噬细胞
CAR-巨噬细胞(CAR-M)被认为是一种有前途的细胞疗法类型。与CAR-T和CAR-NK细胞相似,CAR-M细胞由识别特定肿瘤抗原的细胞外信号传导域、跨膜区域和细胞内激活信号区域组成。目前,对细胞外信号域的研究主要是常见的肿瘤靶点,如CD19和HER2等。比起T细胞和NK细胞等免疫细胞,巨噬细胞可能在免疫抑制性微环境中更容易浸润肿瘤,为肿瘤免疫治疗提供了新的机会。
现已开发出具有识别癌胚抗原相关细胞粘附分子5(CEACAM5)、CD19、CD22、HER2和CD的受体的人类CAR-M,以攻击造血和实体肿瘤(图4)
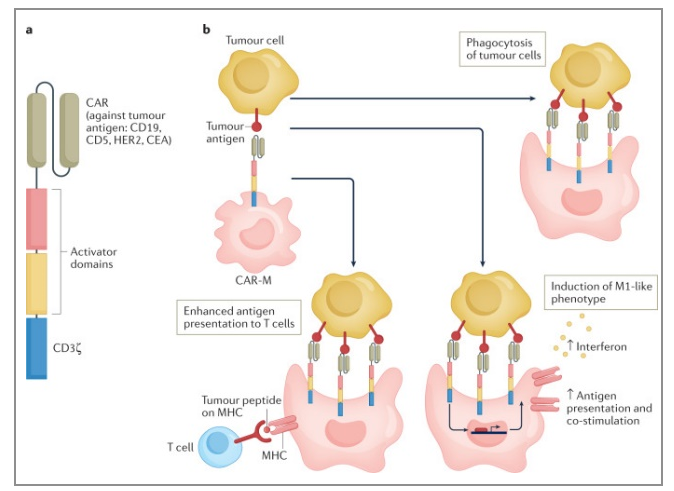
Figure 4 Macrophages as tools and targets in cancer therapy 基于CAR-M的细胞疗法
△点击放大图片
总结
肿瘤相关巨噬细胞在血管生成、细胞外基质重塑、癌细胞增殖、转移和免疫抑制以及对化疗药物和检查点阻断免疫疗法的抵抗中均发挥着重要作用。清除TAMs,阻止TAMs招募,TAMs复极化均是常见的策略。
当然,现在每种策略还有其局限性,相信在未来高选择性药物的开发将有助于推动靶向TAMs的抗肿瘤免疫治疗进一步发展。
主要参考文献:
1. Anna Maria Malfitano et al,Tumor-Associated Macrophage Status inCancer Treatment,Cancers 2020, 12, 1987
2. Wang LX, et al,M2b macrophage polarization and its roles in diseases, J Leukoc Biol. 2019 Aug;106(2):345-358.
3. Mantovani A, et al. Macrophages as tools and targets in cancer therapy,Nat Rev Drug Discov. 2022. Nov;21(11):799-820.
4. Mantovani A, et al. Next frontier in tumor immunotherapy: macrophage-mediated immune evasion. Nat Rev Drug Discov. 2022. Nov;21(11):799-820.
部分相关产品:
| 产品 | 货号 |
| Human IL-10 Antibod | AF-217 |
| Human CCL2/JE/MCP-1 Antibody | MAB2791 |
| Human CCL18/PARC Antibody | AF394 |
| Human CCL17/TARC Antibody | MAB3641 |
| Human CXCL4/PF4 Antibody | MAB7952 |
| CCL18 (MIP-4) Antibody, anti-human, PE, REAfinity™ | 130-126-552 |
| CCL18 (MIP-4) Antibody, anti-human, APC, REAfinity™ | 130-107-609 |
| Human CD47 Antibody | AF4670 |
| Human CD47 PE-conjugated Antibody | FAB4670P |
| CD11b MicroBeads, human, mouse | 130-049-601 |
| CD14 MicroBeads, human | 130-050-201 |
| MidiMACS Starting Kit | 130-042-301 |