在此次抗疫工作中,干细胞应用于新冠肺炎,临床治疗取得了良好成果。使得干细胞的研究成为焦点,其中间充质干细胞因具有多向分化、免疫调节、分泌细胞外囊泡体等特点应用更为广泛。越来越多的研究表明,间充质干细胞来源外泌体与间充质干细胞有着相似的功能,包括修复与再生组织、抑制炎症反应及调节机体免疫等,但外泌体相对于间充质干细胞有更稳定,更好保存,易于控制的优势。因此间充质干细胞外泌体的相关研究进入更多人的视线,期待MSCs外泌体更多的研究成果,带来更先进的疾病医疗手段。小优也整理了几篇相关文献
文章一
Exosomes Derived From miR-133b-Modified Mesenchymal Stem Cells Promote Recovery After Spinal Cord Injury.
文章
△点击放大图片
研究间充质干细胞外泌体介导的miRNA-133的递送对SCI治疗。作者将miR-133b包装到间充质干细胞分泌的外泌体中。诱发大鼠脊髓损伤(SCI)后,向其尾静脉注射miR-133b外泌体,与对照组相比miR-133b外泌体激活了ERK1/2,STAT3和CREB(参与神经元存活和轴突再生的信号通路蛋白)显著改善SCI后后肢运动功能的恢复。
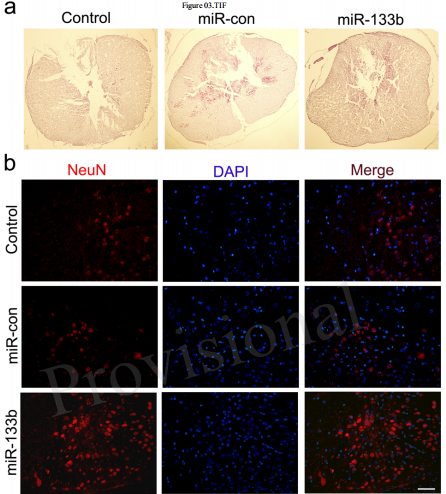
△点击放大图片
注射mir-133b外显子可减少SCI后病变体积,保留Neun神经元

△点击放大图片
miR-133b外泌体对GAP43,NF,RhoA,pERK1 / 2,p-CREB和p-STAT3表达水平的影响。Western印迹显示,miR-133b外泌体增加了GAP43(a)和NF(b)的表达,降低了RhoA(c)的表达,并且促进SCI后受损脊髓中的ERK1 / 2(d),CREB(e)和STAT3(f)的磷酸化
文章二
Thrombin Preconditioning of Extracellular VesiclesDerived from Mesenchymal Stem Cells AcceleratesCutaneous Wound Healing by Boosting TheirBiogenesis and Enriching Cargo Content.

△点击放大图片
研究了间充质干细胞(MSC)的细胞外囊泡体(EV)用于创面修复的最佳预处理方式。作者通过用凝血酶(40 U),H2O2(50 µM),脂多糖(1 µg / mL)或低氧(10%O2)预处理MSC衍生的EV,通过Elisa测量蛋白来定性定量评估EV分泌,通过检测体外人脐带血内皮细胞(HUVEC)的增殖,迁移和管形成,定量皮肤伤口愈合程度来评估EVs的治疗功效。得出凝血酶预处理可最佳地提高EV的产生,并丰富EV中包括血管内皮生长因子和血管生成素的各种生长因子。凝血酶预处理可通过pERK1/2和pAKT信号通路在体外最佳的增强HUVEC的增殖,迁移和管形成,并在体内加速皮肤伤口愈合方面最有效。和其他几种处理方式比较表现出最佳的治疗效果。

△点击放大图片
带有多种预处理的MSC的内体和表征EV。分别用凝血酶(40 U),低氧(10%O2),LPS(1 µg)或H2O2(50 µM)预处理MSC。
(A)MSC的代表性TEM图像。在凝血酶预处理组中,在细胞膜附近大量观察到许多外泌体(黑色箭头),而在其他组中则稀疏地观察到(上图)。尽管在所有预处理组的MSC中都很好地观察到了内体(星号),但在凝血酶处理的MSC中观察到的EV数量更多(下图)
(B)在MSC中用CellLight早期内体-GFP标记的早期内体。内体用GFP(绿色)标记,核用DAPI(蓝色)标记。
(C)使用Zetasizer的外泌体的粒度分布。Y轴表示EV的数量,X轴表示通过Zetasizer分析的EV的尺寸
(D)在各种预处理条件下培养的MSC分离出的EV的平均大小。(n = 5)
(E)从以各种预处理状态培养的MSC中分离出的EV的代表性SEM(左图)和TEM(右图)
(F)代表来自MSCs和MSC来源的EV的细胞器标记蛋白的Western blot,代表线粒体标记的细胞色素C,代表核标记的原纤维蛋白,代表Golgi装置标记的GM130和代表外泌体标记的CD63和CD9

△点击放大图片
△点击放大图片
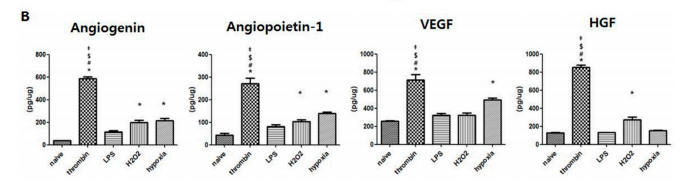
在不同的伤口模拟环境刺激后,外泌体包含各种细胞因子和趋化因子。从经凝血酶(40 U),LPS(1 µg),H2O2(50 µM)或低氧(O2 10%)预处理的MSC中分离出EV。
(A)蛋白质组分析仪人血管生成阵列(PPHAA)的EV蛋白质货物的代表性X线胶片印迹分析(上图)及其代表的图表,通过用与天真的小组。灰色的点线表示比纯稚组增加了三倍
(B)在外泌体中通过多重ELISA测定的血管生成素,血管生成素-1,VEGF和HGF的水平。使用单向方差分析(ANOVA)进行统计分析。星号(*)表示与纯电动车相比p <0.05,数字符号(#)表示与10%氧气处理的电动车相比p <0.05,双匕首(‡)表示与H2O2-相比p <0.05治疗的EV组,与LPS治疗的EV组相比,美元符号($)表示p <0.05(每次分析n = 5)

△点击放大图片
从体内相同数目的MSC(5×105)分离出的EV的伤口愈合能力比较。用生理盐水,天真外泌体,10%O2外泌体,凝血酶(40 U)外泌体,LPS(1 µg)外泌体或源自相同数量MSC的H2O2(50 µM)外泌体局部打孔。
(A)体内代表性的连续伤口图像
(B)治疗2、4、6和8天后的相对伤口闭合率(%)
(C)在每次处理后四天和八天,对切开的伤口组织匀浆中的TNF-α和IL-6β进行细胞因子分析。数据表示为平均值±SEM。使用单向方差分析(ANOVA)进行统计分析。星号(*)表示与盐水相比p <0.05,数字符号(#)表示与纯电动车组相比p <0.05(每次分析n = 4)
间充质干细胞外泌体的相关研究还有很多,例如:含有miR-140-5p的滑膜间充质干细胞来源外泌体(SMSC-Exo)可影响软骨组织再生;骨髓间充质干细胞来源外泌体携带的miR-196a可调节成骨细胞分化促进大鼠颅骨缺损的骨再生。外泌体还可作为疾病诊断标记物、调控靶细胞功能、参与细胞生物学活动等。相关实验展开如:高质量的外泌体分离与干细胞的培养都是研究的关键。
外泌体提取方法对比

△点击放大图片
产品推荐
1 外泌体分离提取产品
| 产品用途 | 货号 | 产品名称 | 规格 |
| 超滤法分离 | 28932237 | Vivaspin 500/2/6/20超滤管 | 500 u-20 ml |
| 超滤法分离 | UFC500396 | Amicon Utra超滤管-3 kDa | 0.5-15 mL |
| 超滤法分离 | UFC510096 | Amicon Ultra超滤管-100kDa | 0.5-15 mL |
| 密度梯度离心 | 17089109 | PERCOLL | 6×1L |
| 密度梯度离心 | 17089102 | PERCOLL | 250ML |
| 柱膜/层析法分离 | 76064 | exoEasy Maxi Kit(20) | 4 ml-16ml |
| 柱膜/层析法分离 | 130-110-912 | Exosome Isolation Kit Pan, human | EA |
| 柱膜/层析法分离 | K1237 | ExosomeIsolation Kit(Cell Media) | 2,10T |
| 柱膜/层析法分离 | 17548115 | HiScreen Capto Core 700 | 1*4.7ml |
| 柱膜/层析法分离 | 17548102 | Capto Core 700 | 100ml |
| 沉淀法分离 | 76603 | mRCURY Exosome Serum/Plasma Kit | 16/50T |
| 沉淀法分离 | M1001 | ExoPureTMReagent(Overall Exosome Isolation) | 25/50T |
| 免疫磁珠法分离 | NBP2-49826-10Reactio | Overall Exosome Isolation(Cell Media) | 10/20 Reactions |
| 免疫磁珠法分离 | M1030 | Overall Exosome Isolation(Cell Media) | 10/20Reactions |
| 免疫磁珠法分离 | NBP2-49835-10Reactio | Overall Exosome Isolation(Biofluids) | 10 Reactions |
| 免疫磁珠法分离 | M1038 | Overall Exosome Isolation(Biofluids) | 20 Reactions |
| 免疫磁珠法分离 | NBP2-498303-10Reactio | Tumor-Derived Exosome Isolation (Biofluids) | 10 Reactions |
| 免疫磁珠法分离 | M1033 | Tumor-Derived Exosome Isolation (Biofluids) | 20 Reactions |
| 外泌体标准品 | M1041 | ExoStdMLyophilized Exosome Standard (100 pg HumanPlasma,2 vials) | 100 ug |
| 外泌体标准品 | M1043 | ExoStdIM Lyophilized Exosome Standard (100ug Human Serum, 2 vials) | 100 ug |
| 外泌体标准品 | M1073 | ExoStdIM Plasma Fluorescent Exosome Standard(9/25/2019) | 100ug |
2 干细胞培养与检测相关产品
| 产品用途 | 货号 | 产品名称 | 规格 |
| 冻存 | PT-2501 | 人间质干细胞hMSC冻存 | 750000cells |
| 维持培养基 | PT-3001 | 间质干细胞生长培养基(包含PT-3238&PT-4105) | Kit |
| 维持培养基 | 190632 | MSCGM-CD;限定化学成分间充质干细胞培养基;(含L-谷氨酰胺,不含酚红和抗生素) | Kit |
| 维持培养基 | BEBP12-725F | UtraCULTURETMSerum-freeCellCultureMedium无血清培养基 | 500mL |
| 维持培养基 | 15950-017 | UtroserSerumSubstitute血清替代物 | 20mL |
| 维持培养基 | abs9401-100ml | Xeno-Free人间充质干细胞培养基(无酚红) | 100ml |
| 维持培养基 | abs9419-500ml | 人脐带间充质干细胞无血清培养基(无酚红) | 500ml |
| 分化培养基 | PT-3002 | 人间质干细胞成骨分化培养基(包含PT-3924&PT-4120) | kit |
| 分化培养基 | PT-3003 | 人间质干细胞软骨分化培养基(包含PT-3925&PT-4121) | kit |
| 分化培养基 | PT-3004 | 人间质干细胞脂肪形成分化培养基(PT3102B,3102A,4122,4135) | kit |
| 基质胶 | abs9410-100ml | 即用型基质胶 | 100ml |
| MSC间充质干细胞扩增分化所需蛋白 | 355-BM-010 | BMP-2 | 10ug |
| MSC间充质干细胞扩增分化所需蛋白 | 314-BP-010 | BMP-4 | 10ug |
| MSC间充质干细胞扩增分化所需蛋白 | 507-BP-020 | BMP-6 | 20ug |
| MSC间充质干细胞扩增分化所需蛋白 | 236-EG-01M | EGF | 1mg |
| MSC间充质干细胞扩增分化所需蛋白 | 233-FB-025 | FGFbasic | 25ug |
| MSC间充质干细胞扩增分化所需蛋白 | 235-F4-025 | FGF4 | 25ug |
| MSC间充质干细胞扩增分化所需蛋白 | 8340-G5-050 | GDF-5/BMP-14 | 50ug |
| MSC间充质干细胞扩增分化所需蛋白 | 259-HE-050 | HB-EGF | 50ug |
| MSC间充质干细胞扩增分化所需蛋白 | 291-G1-200 | IGF-1 | 200ug |
| MSC间充质干细胞扩增分化所需蛋白 | 7270-IL-025 | IL-6 | 25ug |
| MSC间充质干细胞扩增分化所需蛋白 | 8335-G1-200 | LR3IGF-1 | 200ug |
| MSC间充质干细胞扩增分化所需蛋白 | 7754-BH-005 | TGF-β1 | 5ug |
| MSC间充质干细胞扩增分化所需蛋白 | 302-B2-002 | TGF-β2 | 2ug |
| MSC间充质干细胞扩增分化所需蛋白 | 8420-B3-025 | TGF-β3 | 25ug |
| MSC间充质干细胞扩增分化所需蛋白 | 7196-WN-010 | Wnt-10b | 10ug |
| MSC间充质干细胞扩增分化所需蛋白 | 6076-WN-005 | Wnt-4 | 5ug |
| MSC间充质干细胞扩增分化所需蛋白 | 7347-WN-025 | Wnt-5b | 25ug |
| 干细胞扩增分化 | 2840/50 | AICAR诱导MSC分化为成骨细胞 | 50mg |
| 干细胞扩增分化 | 4918/10 | GSA10诱导MSC分化为成骨细胞 | 10mg |
| 干细胞扩增分化 | 4551/10 | Purmorphamne诱导MSC分化为成骨细胞 | 10mg |
| 干细胞扩增分化 | 1126/100 | Dexamethasone诱导MSC分化为脂肪细胞 | 100mg |
| 干细胞扩增分化 | 2845/50 | IBMX诱导MSC分化为脂肪细胞 | 50mg |
| 干细胞扩增分化 | abs9406-100ml | 人间充质干细胞成软骨分化试剂盒 | 100mL |
| 干细胞扩增分化 | abs9407-100ml | 人间充质干细胞成脂分化试剂盒 | 100mL |
| 干细胞扩增分化 | abs9408-100ml | A间充质干细胞成骨分化试剂盒 | 100mL |
| 分化鉴定 | abs9414-100ml | 成脂检则染液 | 100mL |
| 分化鉴定 | abs9415-100ml | 成骨检则染液 | 100mL |
| 分化鉴定 | abs9416-100ml | 成软骨检则染液 | 100mL |
| 成脂ELISA检则 | DY1065 | humanAdiponectin/Acrp30 DuosetELISA | 1 kit |
| 成脂ELISA检则 | DRP300 | humanAdiponectin/Acrp30 QuartikineELISA | 1 kit |
| 成脂ELISA检则 | DLP00 | humanLeptin QuarikineELISA | 1 kit |
| 成软骨ELISA检测 | DY1220 | humanAggrecan DuosetELISA | 1 kit |
| 成软骨ELISA检测 | DSP00 | humanSPARC/Osteonectin QuantikineELISA | 1 kit |
| 成软骨ELISA检测 | DSTCN0 | humanOsteocalcin QuartikineELISA | 1 kit |
| 成软骨ELISA检测 | DOST00 | humanOsteopontin QuartikineELISA | 1 kit |
| 成软骨ELISA检测 | DY6220-05 | humanPro-CollagenIa1 DuosetELISA | 1 kit |
| 成软骨ELISA检测 | DSP00 | humanSPARC/Osteonectin QuantikineELISA | 1 kit |
| 抗体芯片检则 | ARY024 | ProteomeProfilerHumanAdipokineArrayKit | 4T |
| 抗体芯片检则 | ARY022B | ProteomeProfilerXLHumanCytokineArrayforOsteogenesis | 4T |
| Luminex检则 | 12007283 | Human Cytokine Screening 48-Plex Services | 1 kit |
| Luminex检则 | 12009159 | Mouse Chemokine Panel 31-Plex Services | 1 kit |
| Luminex检则 | 12005641 | Rat Cytokine 23-Plex Services | 1 kit |
| MSD检测 | K15049D-1 | V-.PLEX Proinflammatory Panel 1 (Human)Kit 10-plex | 1 kit |
| MSD检测 | K15048D-1 | V.PLEXProinflammatory Panel 1 (Mouse)Kit 10-plex | 1 kit |
| MSD检测 | K15059D-1 | V-PLEX Proinflammatory Panel 2 Rat Kit | 1 kit |
3 miRNA整套方案产品
| 产品用途 | 货号 | 产品名称 | 规格 |
| 纯化 | 77064 | exoRNeasy Serum/Plasma Maxi Kit(5o) | 50Test |
| PCR检测 | 218161 | miScript IIRT Kit (5o) | 50Test |
| PCR检测 | 218073 | miScript SYBR Green PCR Kit(20o) | 200Test |
| NGS检测 | 331505 | QIAseq miRNA Library Kit (96) | 96 |
| NGS检测 | 333714 | QIAseq 12-Index I (48) | 12 |
| NGS检测 | 333314 | QIAseq Library Quart Assay Kit | 12 |
| 分析软件 | 830008 | IPA with Advanced Analytics NUL | EA |
参考文献
LI D, ZHANG P, YAO X, et al. Exosomes Derived From miR-133b-Modified Mesenchymal Stem Cells Promote Recovery After Spinal Cord Injury. Front Neurosci. 2018;12:845.
LOU G H,CHEN Z,ZHENG M,et al. Mesenchymal stem cell-derived exosomes as a new therapeutic strategy for liver diseases[J]. Exp Mol Med,2017,49( 6) : e346.
Dong Kyung Sung , Yun Sil Chang.Thrombin Preconditioning of Extracellular Vesicles Derived from Mesenchymal Stem Cells Accelerates Cutaneous Wound Healing by Boosting Their Biogenesis and Enriching Cargo Content[J]J. Clin. Med. 2019, 8, 533.
罗雅馨,毕浩然.间充质干细胞来源外泌体与再生医学:无细胞疗法临床应用的未来.[J]中国组织工程研究,2020,24(19):3055-3062.
杜月,顾永卫.间充质干细胞外泌体作为药物递送载体的研究进展[J]中国药学杂志 2020,1 ,55 (1),1-7.