实验步骤
- 1
- 2
- 3
- 4
- 5
- 6
-
蛋白制备
使用缓冲液制备4X初始浓度的蛋白X和Y。蛋白:实验室纯化获得或商业化蛋白,蛋白浓度已知;
-
蛋白稀释
按照最高浓度进行10倍连续稀释(仅包括缓冲液样品):
PROTEIN X Tube # Final Concentration 4X Concentration 1 300 nM 1200nM 2 30 nM 120 nM 3 3nM 12 nM 4 OnM 0 nM PROTEIN X Tube # Final Concentration 4X Concentration 1 300 nM 1200 nM 2 30 nM 120 nM 3 3nM 12 nM 4 OnM 0 nM 图2:抗体对选择实验蛋白稀释参考
-
加样
以384孔板为例,取微孔板平置于操作台,以5μl/孔加入蛋白X(4X)后,加入蛋白Y(4X),盖上封板膜(防止样本蒸发),室温静置,孵育60分钟。
Tips 1:如果没有信号或信号很低,可考虑增加或降低孵育温度将提高信号,而不增加背景。
Tips 2:孵育时间可依据蛋白特性进行优化调整,延长或缩短时间,多数蛋白样本60分钟时间足够。
-
加检测试剂
每孔加入5μl抗标签供体和5μl抗标签供体。(或可将检测试剂预混在一起,后以10μl/孔加入样本中)。盖上封板膜,室温静置,孵育60分钟。
Tips 1:在第一次实验时,可选择在120、180、240分钟和夜间进行多次检测,以获得最佳测检测信号。
-
读板
去掉封板膜,平行放入酶标仪,选择TR-FRET程序进行读值。
-
结果
最好的信噪比,即信号/背景(S/B),作为蛋白的最佳浓度。
举例:6His-p53蛋白和GST-HDM2蛋白相互作用, anti-GST-d2和anti-6His-Tb Gold获得最佳信噪比,为最佳抗体配对。(如图3)
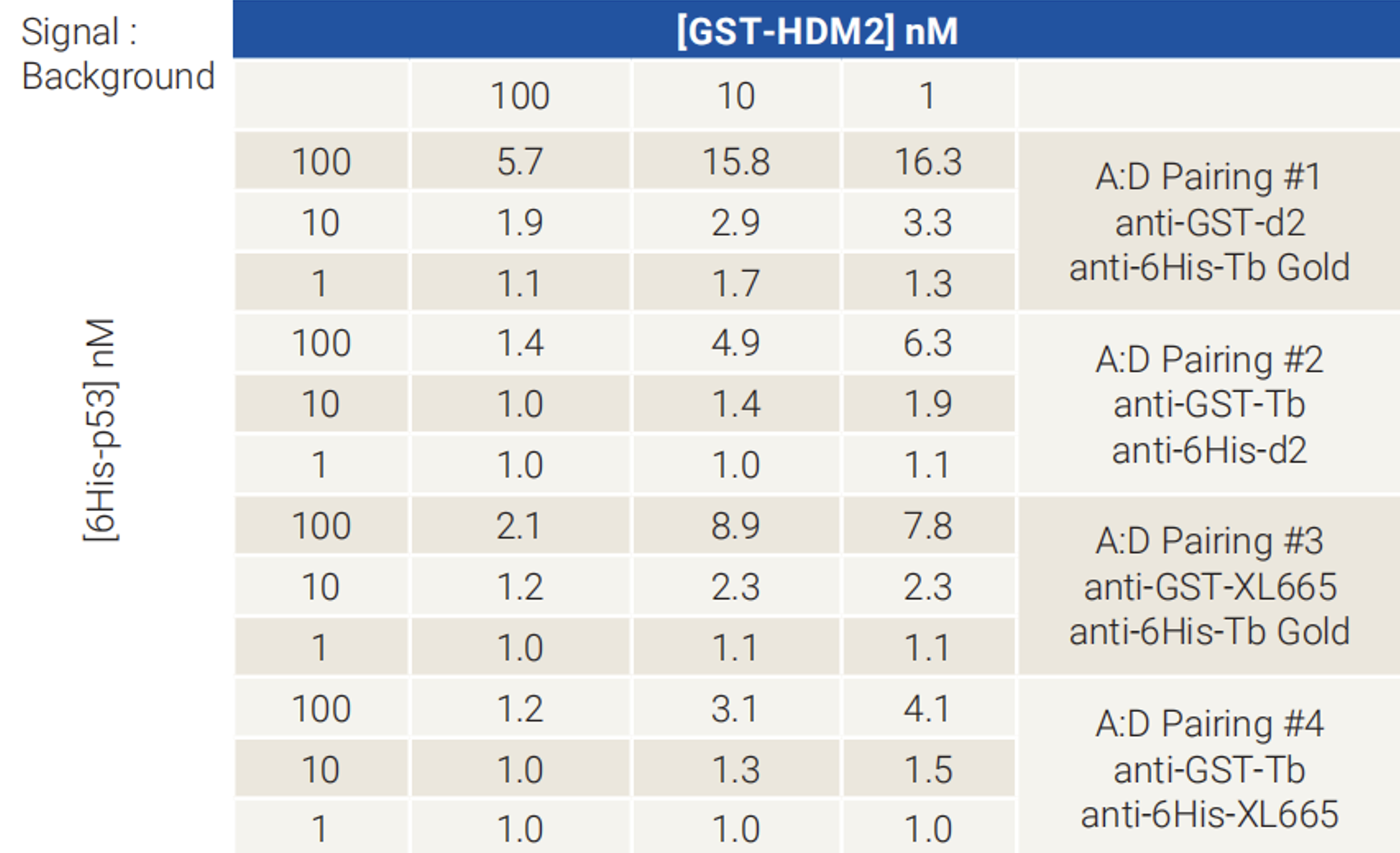
图3:p53-HDM2案例分析
△点击放大图片

